حصہ 1: مائٹوکونڈریو پیتھیز اور اس سے وابستہ پیتھالوجیز کے خلاف فلیوونائڈز کے حفاظتی اثرات: پیشن گوئی کے نقطہ نظر اور ذاتی نوعیت کی روک تھام پر توجہ مرکوز کریں
Mar 31, 2022
مزید معلومات کے لیے۔ رابطہtina.xiang@wecistanche.com
خلاصہ: ملٹی فیکٹوریل مائٹوکونڈریل نقصان ایک "شیطانی دائرے" کو ظاہر کرتا ہے جو مائٹوکونڈریل dysfunction اور کثیر اعضاء کے منفی اثرات کی ترقی کا باعث بنتا ہے۔ مائٹوکونڈریل خرابیاں (مائٹوکونڈریو پیتھیس) شدید پیتھالوجیز سے وابستہ ہیں جن میں کینسر، قلبی امراض، اور نیوروڈیجنریشن شامل ہیں لیکن ان تک محدود نہیں۔ تاہم، کاسکیڈنگ پیتھالوجیز کی قسم اور سطح انتہائی انفرادی ہے۔ اس کے نتیجے میں، مریض کی سطح بندی، خطرے کی تشخیص، اور تخفیف کے اقدامات لاگت سے مؤثر انفرادی تحفظ کے لیے اہم ہیں۔ لہذا، رد عمل سے پیشین گوئی، روک تھام، اور ذاتی ادویات (3 PM) کی طرف مثالی تبدیلی جدید صحت کی دیکھ بھال میں ناگزیر ہے۔فلاوونائڈز واضح مظاہرہاینٹی آکسیڈینٹاور صفائی کی سرگرمی مائٹوکونڈریل نقصان اور جھرنے والی پیتھالوجیز کے خلاف بہترین علاج کی افادیت ہے۔ 3 PM کے تناظر میں، یہ جائزہ مائٹوکونڈریو پیتھیز اور اس سے منسلک پیتھالوجیز کے خلاف ایک طاقتور محافظ کے طور پر flavonoids کی افادیت کا جائزہ لینے والے preclinical اور کلینیکل ریسرچ ڈیٹا پر توجہ مرکوز کرتا ہے۔
مطلوبہ الفاظ: قدرتی مادہ؛ فائٹو کیمیکل؛ flavonoids؛ اینٹی آکسیڈینٹ سرگرمی؛ جینو پروٹیکشن؛ تناؤ؛ مائٹوکونڈریل خرابی؛ mitochondriopathy؛ mitochondrial تقریب؛ dysfunction چوٹ؛ tumorigenesis؛ کینسر دل کی بیماری؛ نیوروڈیجنریشن؛ پیشن گوئی سے بچاؤ کی ذاتی دوا (PPPM/3PM)؛ مریض کی سطح بندی

1. تعارف
بائیو اینرجیٹکس اور سیل بائیولوجی میں مائٹوکونڈریل فنکشن اور ڈیسفکشن کی اصطلاحات بڑے پیمانے پر استعمال ہوتی ہیں۔ مائٹوکونڈریل عمل میں اسامانیتا، بشمول اڈینوسین ٹرائی فاسفیٹ (اے ٹی پی) جنریشن، اپوپٹوسس، سائٹوپلاسمک اور مائٹوکونڈریل میٹرکس کیلشیم ریگولیشن، ری ایکٹیو آکسیجن اسپیسز (آر او ایس) جنریشن اور ڈیٹوکسیفیکیشن، میٹابولائٹ سنتھیسز، اور انٹرا سیلولر ٹرانسمیشن ٹرمیشنز۔ Mitochondrial dysfunction دماغ، پٹھوں، ریٹنا، cochlea، جگر، اور گردے سمیت مختلف اعضاء اور بافتوں کو متاثر کرتا ہے، جو آکسیڈیٹیو فاسفوریلیشن (OXPHOS) کی خرابیوں کے لیے سب سے زیادہ حساس ہوتے ہیں۔ مائٹوکونڈریل عوارض (مائٹوکونڈریو پیتھیز) کے مریضوں میں مختلف علامات ظاہر ہوتی ہیں، جن میں بہرا پن، بصارت کی خرابی، دل، جگر اور گردے کے مسائل، فالج، درد شقیقہ، ذیابیطس، مرگی، ایٹیکسیا، موٹر اور دماغی نشوونما میں تاخیر، اور نشوونما پانے میں ناکامی، یہ سب شامل ہیں۔ متعدد غیر مائٹوکونڈریل عوارض میں اکثر مشاہدہ کیا جاتا ہے [2]۔ لہٰذا، مائٹوکونڈروپیتھیز کا موثر انتظام طب میں ایک بڑا چیلنج ہے۔
فی الحال، مائٹوکونڈریل عوارض کی تشخیص فنکشنل اسٹڈیز، کلینیکل، بائیو کیمیکل، اور ہسٹوپیتھولوجک امتحانات، اور سالماتی جینیاتی جانچ [3] کی بنیاد پر کی جاتی ہے۔ تاہم، خلیے سے پاک نیوکلک ایسڈز یا بائیو فلوئڈز جیسے خون، پیشاب، تھوک، دماغی مادہ، پسینہ، یا آنسو استعمال کرنے والی تشخیصی تکنیک ناگوار ٹشو بایپسی [4-7] کی جگہ لے سکتی ہیں۔ رد عمل سے پیش گوئی کرنے والی، روک تھام اور ذاتی دوا (3 PM) کی طرف نمونہ کی تبدیلی صحت کی دیکھ بھال کے طریقوں پر مبنی ہے جو ٹارگٹڈ احتیاطی اقدامات کا فائدہ اٹھاتے ہیں جو کہ دائمی بیماریوں اور طبی خدمات کے اخلاقی اور معاشی پہلوؤں کا سبب بنتے ہیں [8,9].3 PM بھی اس میں مریض کی انفرادی پروفائلنگ شامل ہے، جو کہ مریض کی سطح بندی، انفرادی رجحان کی خصوصیت، اور ذاتی نوعیت کے علاج کے لیے اہم ہے [10]۔ مزید برآں، کثیر سطحی تشخیصی طریقوں میں سالماتی حیاتیاتی خصوصیت، ناول eHealth پر مبنی تشخیصی ٹولز، سوالنامے، اور طبی امیجنگ شامل ہیں [9]۔
حالیہ برسوں میں، قدرتی طور پر پائے جانے والے پولی فینولک مرکبات، فلیوونائڈز کے صحت مند اثرات نے طبی تحقیق کو اپنی طرف متوجہ کیا ہے، جس میں مائٹوکونڈریل خرابیوں سے منسلک پیتھالوجیز میں ان کا استعمال بھی شامل ہے [11] جیسے کینسر، قلبی اور نیوروڈیجنریٹیو امراض[12]۔ flavonoids کی افادیت کو وسیع پیمانے پر پری کلینیکل شواہد کی حمایت حاصل ہے جو 3 PM اپروچ [13-19] کے مطابق mitochondriopathies کے مخصوص ٹارگٹڈ اور پرسنلائزڈ تھراپی میں ان مرکبات کے ممکنہ مستقبل میں استعمال کے بارے میں مزید تحقیق کی بنیاد کی نمائندگی کرتا ہے۔
یہ جائزہ مائٹوکونڈریو پیتھیوں میں فلیوونائڈز کی افادیت پر تبادلہ خیال کرتا ہے۔کینسر, قلبی امراض(CVDs)، اور neurodegenerative عارضے، 3 PM کے جدید نفاذ کی ضرورت کو اجاگر کرتے ہیں۔

2. مائٹوکونڈریل نقصان اور اس سے وابستہ خرابیاں
یوکرائیوٹک جانداروں میں، مائٹوکونڈریا کا سیلولر افعال جیسے کہ توانائی کے تحول، بایو سنتھیسس، آئنک ریگولیشن، آکسیڈیشن اور/یا کمی، اور سیل کمیونیکیشن، عمر بڑھنے، مدافعتی ردعمل، اپوپٹوسس، بقا، اور موت سے وابستہ سگنلنگ راستے میں ایک ضروری کردار ہوتا ہے [12] . مائٹوکونڈریا کے بنیادی افعال OXPHOS کے ذریعے ATP کی ترکیب، کربس سائیکل کے ذریعے میٹابولائٹ آکسیکرن، اور فیٹی ایسڈ آکسیڈیشن [20] ہیں۔ مائٹوکونڈریل جینوم کلیدی الیکٹران ٹرانسپورٹ چین (ETC) پروٹین کو انکوڈ کرتا ہے جو ایروبک جانداروں میں توانائی کی پیداوار میں اہم کردار ادا کرتے ہیں [21]۔ ہیومن مائٹوکونڈریل ڈی این اے (ایم ٹی ڈی این اے) ایک ڈبل سٹرینڈڈ سرکلر مالیکیول ہے جو 16,569 بیس جوڑوں پر مشتمل ہوتا ہے [22]۔ عام حالات میں، مائٹوکونڈریا میں اپنے ڈی این اے کی متعدد کاپیاں (100 سے 10،{10}} فی سیل) ہوتی ہیں [23]۔
ای ٹی سی آر او ایس اور ری ایکٹیو نائٹروجن اسپیسز (آر این ایس) کا بھی ایک ذریعہ ہے، او ایکس پی او ایس کی ضمنی مصنوعات جو ڈی این اے، آر این اے اور پروٹین کو نقصان پہنچاتی ہیں [24]۔ خراب ایم ٹی ڈی این اے کی مرمت کے لیے بیس ایکسائز ریپیر (BER) کی نااہلی ROS پروڈکشن سے منسلک ETC رکاوٹ کا باعث بنتی ہے (شکل 1 میں دکھایا گیا ہے)۔ مزید یہ کہ ای ٹی سی کی سرگرمی متعدد مائیلوما کے مریضوں میں منشیات (وینیٹوکلاکس) کی حساسیت کے پیش گو اور ہدف کے طور پر بھی کام کر سکتی ہے [25]۔ مزید یہ کہاوکسیڈیٹیو تناؤand insufficient DNA damage repair could increase DNA damage resulting in mitochondrial dysfunction in patients with depression. Therefore, a marker 8-oxoguanine of oxidative DNA damage obtained from fluid biopsies (blood, urine) could be beneficial for the prevention and prediction of neurodegenerative disorders such as mito chondriopathies [26]. Subsequently, extensive oxidative mtDNA damage manifests in several mitochondrial dysfunctions and diseases [27]. Mitochondrial dysfunctions can also be caused by mtDNA mutations, deletions, and impaired DNA replication (shown in Figure 1)[28]. For example, the mtDNA m.3243A>G اتپریورتن دو کلینیکل سنڈروم سے متعلق کلینیکل فینوٹائپس کا باعث بن سکتی ہے: زچگی سے وراثت میں ملنے والی ذیابیطس اور بہرا پن (MDD)، اور mitochondrial encephalomyopathy، lactic acidosis، اور strokelike episode (MELAS) سنڈروم [29]۔ مزید یہ کہ ایم ٹی ڈی این اے اتپریورتنوں سے وابستہ مائٹوکونڈریل سنڈروم کی کچھ طبی خصوصیات میں مائٹوکونڈریل وراثت کے زچگی کے انداز کی وجہ سے زچگی کی خاندانی تاریخ شامل ہے۔ متفقہ انسانی ترتیب کی دستیابی کی وجہ سے مائٹوکونڈریل جینوم کی ترتیب کے تجزیہ کی سادگی وراثت کے لحاظ سے ایم ٹی ڈی این اے کی خرابیوں کو پہچاننے میں مدد کر سکتی ہے۔ مائٹوکونڈریل dysfunction کے ساتھ منسلک دیگر mtDNA تغیرات عمر بڑھنے کے عمل کے ذریعے زندگی کے دوران حاصل کیے جاتے ہیں۔ یہ حاصل شدہ mtDNA اتپریورتنوں کا تعلق اکثر عمر سے متعلقہ بیماریوں جیسے ذیابیطس سے ہوتا ہے۔ لہذا، بنیادی مائٹوکونڈریل جینیات کی تفہیم میں پیش رفت کو وراثتی مائٹوکونڈریل اتپریورتنوں اور بیماری کے فینوٹائپس کے درمیان تعلق کے تجزیہ کے لیے ایک اہم ذریعہ سمجھا جاتا ہے جس کے ذریعے حاصل شدہ mtDNA اتپریورتنوں [30,31] کی نشاندہی کی جاتی ہے۔ ایم ٹی ڈی این اے کی دیکھ بھال کے ساتھ منسلک جوہری جینوں کی مختلف حالتیں، بشمول انکوڈنگ ایم ٹی ڈی این اے ریپلیکیشن انزائمز، وہ پروٹین جو مائٹوکونڈریل نیوکلیوٹائڈ پول کی دیکھ بھال میں کام کرتے ہیں، اور وہ پروٹین جو مائٹوکونڈریل فیوژن میں حصہ لیتے ہیں (شکل 1 میں دکھایا گیا ہے)[32]۔ اس کے علاوہ، عمر بڑھنے کا عمل مائٹوکونڈریل بائیوجنسیس (فیوژن اور فیوژن) میں کمی سے منسلک ہے اور غیر فعال مائٹوکونڈریا کو ختم کرنے کے ایک اہم عمل میں بھی جس کی خصوصیات مائٹوفیجی ہے [20]۔ مزید یہ کہ، mtDNA اتپریورتنوں کے واقعات اور تعدد عمر کے ساتھ نمایاں طور پر بڑھتے ہیں، جو سیلولر سنسنی [33] میں حصہ ڈالتے ہیں۔

جیسا کہ اوپر بحث کی گئی ہے، مائٹوکونڈریل خرابیاں ان کی مختلف طبی خصوصیات اور جینیاتی ایٹولوجی کے لحاظ سے مختلف انتہائی متضاد بیماریوں سے وابستہ ہیں۔ لہذا، مائٹوکونڈریل خرابیوں سے وابستہ مالیکیولر میکانزم کا تجزیہ اور/یا وضاحت تشخیص اور مزید طبی انتظام کے لیے چیلنجوں کی نمائندگی کر سکتی ہے [34]۔ آخر میں، مائٹوکونڈریل dysfunction بہت سی بیماریوں کا ایک خاص نشان ہے جو مائٹوکونڈریو پیتھیز کے نام سے جانا جاتا ہے، بشمول خرابی، CVDs، اور نیوروڈیجنریشن۔ لہذا، مائٹوکونڈریل بیماری کے میکانزم کو نشانہ بنانے والے نئے علاج تلاش کرنا ضروری ہے۔
2.1.Mitochondiopaties کینسر کی نشوونما میں ملوث ہیں۔
مائٹوکونڈریا کے اپوپٹوٹک راستوں اور واربرگ فینوٹائپ کے میکانزم میں ضروری کام ہوتے ہیں، ایسے عمل جن کا گہرا تعلق ہےکینسر. مائٹوکونڈریا مائٹوکونڈریل بیرونی جھلی پارمیبلائزیشن، سائٹوکوم سی ریلیز، اپوپٹوسم کی تشکیل، کیسپیس ایکٹیویشن، اور سیل ڈیتھ [35] سے وابستہ اپوپٹوٹک سیل کی موت کے اندرونی راستے میں ایک اہم کردار ادا کرتا ہے۔ Apoptosis کی چوری انسانی کینسر کی نشوونما کی ایک پہچان ہے۔ کینسر کے خلیے بقا کی کئی حکمت عملیوں کا فائدہ اٹھاتے ہیں، بشمول مائٹوکونڈریل اپوپٹوسس کی روک تھام کے ذریعے اینٹی اپوپٹوٹک اور پرو سروائیول سگنلنگ کو چالو کرنا۔ لہذا، اندرونی (مائٹوکونڈریل) اپوپٹوٹک راستے کینسر مخالف حکمت عملیوں کے لیے ایک امید افزا ہدف کی نمائندگی کرتے ہیں [36]۔
1956 میں، اوٹو واربرگ نے اس عمل کو بیان کیا جس کے ذریعے کینسر کے خلیات تیزی سے پھیلنے کو برقرار رکھتے ہیں۔ یہ عمل، جسے واربرگ ایفیکٹ کے نام سے جانا جاتا ہے، نارموکسک حالات میں بھی گلوکوز کی مقدار میں اضافہ اور لییکٹیٹ سراو (ایروبک گلائکولائسز) کی خصوصیت رکھتا ہے، یہ تجویز کرتا ہے کہ مائٹوکونڈریل سانس میں نقائص ٹیومرجینیسیس کو فروغ دے سکتے ہیں [37,38]۔ ستنداریوں میں، پروٹین کناسز (PK) کی ماڈیولیشن، جیسے PKL، PKR، PKM1، اور PKM2، کینسر کے خلیوں میں واربرگ اثر کو بڑھاتی ہے [39]۔ مزید برآں، mtDNA کی کمی چھاتی، گردوں، پروسٹیٹ، اور دیگر کینسروں میں مائٹوکونڈریل فنکشن میں تبدیلی کا باعث بنتی ہے، اور عمر سے متعلقہ امراض، ٹیومرجینیسیس [40-43] میں مائٹوکونڈریا کے کردار کو واضح کرتا ہے۔ مزید برآں، کربس سائیکل انزائمز میں مختلف تغیرات، جن میں سوکسینیٹ ڈیہائیڈروجنیز (SDH)، فومریٹ ہائیڈروٹیز (FH)، اور isocitrate dehydrogenase 1 (IDH1) اور 2 (IDH2) شامل ہیں، کینسر کے خلیوں میں بیان کیے گئے ہیں [44]۔ SDH اتپریورتنوں کا تعلق ہائپوکسیا پاتھ وے ایکٹیویشن سے ہوتا ہے، جو مائٹوکونڈریل فیوژن اور فیوژن، مائٹوفجی اور او ایکس پی ایچ او ایس کو تبدیل کر سکتا ہے۔ اس کے علاوہ، FH اور IDH تغیرات سیلولر تفریق کے جبر کے ذریعے ٹیومر کی شروعات کا باعث بنتے ہیں، اور IDH1 اور DH2 تغیرات کینسر کے خلیوں میں توانائی کی تبدیلی کا سبب بنتے ہیں [45,46]۔ متذکرہ کربس سائیکل انزائمز میں غیر معمولی چیزیں ایک میٹابولائٹس کی پیداوار کے ذریعے سرطان پیدا کرنے کے عمل کو فروغ دیتی ہیں، بشمول 2-ہائیڈرو آکسیگلوٹریٹ اور سائٹریٹ، فیٹی ایسڈ آکسیڈیشن میں اضافہ، اور اپیتھیلیل-میسینچیمل ٹرانزیشن (EMT) انڈکشن [47]۔
مزید برآں، mtDNA میں تغیرات، خاص طور پر کمپلیکس I، IⅢ، IV، اور V کے جینوں میں، جو OXPHOS اور redox ریگولیشن کے ساتھ قریب سے وابستہ ہیں، endometrial، گریوا، چھاتی، اور اپکلا ڈمبگرنتی کینسر کے خلیوں میں دیکھے گئے [44,46,48 ] خاص طور پر، کمپلیکس میں اتپریورتنوں کا تعلق ایک اعلی -ketoglutarate/succinate تناسب سے ہے، جو کہ hypoxia-inducible factor 1 (HIF1) عدم استحکام کے ذریعے ٹیومرجینیسیس کو فروغ دیتا ہے [49]۔ اگرچہ mtDNA میں تغیرات mitochondrial dysfunction اور کینسر کی نشوونما کے امکانات کا باعث بنتے ہیں، یہ تغیرات ریٹروگریڈ سگنلنگ [44] کے ذریعے جوہری جین کے اظہار کو بھی متاثر کرتے ہیں۔

2.2 قلبی امراض میں مائٹوکونڈریل ڈیسفکشن
CVDs عالمی اموات اور بیماری کی سب سے بڑی وجہ ہیں [50]۔ دل کے ہومیوسٹاسس میں مائٹوکونڈریا کا ایک اہم کردار ہے۔ مائٹوکونڈریل مورفولوجی کارڈیو مایوسائٹس [51] میں تبدیلیوں کے لئے جوابدہ ہے۔ مائٹوکونڈریل بیماریاں جو ترجیحی طور پر دل کو متاثر کرتی ہیں ان کا تعلق مائٹوکونڈریل dysfunction سے ہوتا ہے، جیسے OXPHOS یا ETC میں رکاوٹیں[52]۔ مائٹوکونڈریل آرگنیلز میں ساختی اور فعال تبدیلیاں اسکیمک کارڈیو مایوپیتھی، دل کی ناکامی اور فالج کا سبب بنتی ہیں [53]۔
مزید برآں، مائٹوکونڈریل ڈائنامکس میں رکاوٹیں، بشمول مائٹوکونڈریل فیوژن، فِشن، بایوجینیسیس، اور مائٹوفیجی، CVDs کی نشوونما اور بڑھنے کا باعث بنتی ہیں جیسے کہ ذیابیطس کارڈیو مایوپیتھی، ایتھروسکلروسیس، اسکیمیا ریپرفیوژن سے ہونے والے نقصان، کارڈیک ہائپر ٹرافی، اور ہارٹ فیلیئر۔ ایم ٹی ڈی این اے کی بحالی اور نقل کو منظم کرنے والے متعدد جوہری جین، بشمول مائٹوکونڈریل ٹرانسکرپشن فیکٹر A (TFAM)، mtDNA پولیمریز (POLG)، اور PEO1 (Twinkle)، CVDs 【55】 میں تبدیل کیے گئے ہیں۔ اس کے علاوہ، mtDNA اتپریورتن جو mtDNA جین کے اظہار کو غیر منظم کرتے ہیں فالج اور مایوکارڈیل انفکشن کے روگجنن کو فروغ دیتے ہیں [56]۔ مزید برآں، ہائپوکسیا سیلولر میکانزم میں تبدیلیوں کا سبب بنتا ہے جو آکسیڈیٹیو تناؤ اور اس کے نتیجے میں مائٹوکونڈریل dysfunction کا باعث بنتا ہے [57]۔
In patients with atherosclerosis and associated CVDs dysfunctional mitochondria affect cellular respiration and energy production and also act as dangerous ROS generators leading to the induction of apoptosis [58]. The accumulation of ROS and RNS in the heart by dysfunctional mitochondria is associated with several CVDs, including cardiomyopathies and heart failure [59,60]. Interestingly, ROS production caused by TFAM dysfunction is related to mtDNA damage and consequent cardiomyocyte cell cycle arrest resulting in lethal cardiomyopathy [61]. Moreover, the prognosis of cardiomyopathy is poor in children with mitochondrial diseases, especially those with mtDNA defects, including the m.3243A>G mutation in mitochondrially encoded tRNA-Leu(UUA/G)1(MT-TL1), the m.13513G>A mutation in mitochondrially encoded NADH: Ubiquinone oxidoreductase core subunit 5(MT-ND5), the m.8528T>Cmutation in the overlapping region of mitochondrially encoded ATP synthase membrane subunits 6(MT-ATP6) and 8(MT-ATP8), the m.3302A>G mutation in MT-ND1, the m.1644G>mitochondrially encoded tRNA valine (MT-TV) میں تبدیلی، اور BolA فیملی ممبر 3 (BOLA3) اور tafazzin TAZ میں روگجنک تغیرات۔ متذکرہ مائٹوکونڈریل اتپریورتنوں والے بچوں میں کارڈیو مایوپیتھی اور اس سے وابستہ اموات کا خطرہ زیادہ ہوتا ہے۔ لہذا، مائٹوکونڈریل خرابیوں کی تفصیلی فینوٹائپنگ کے ساتھ جینیاتی تجزیہ کارڈیو مایوپیتھی [62] کی تشخیص کے لیے مفید ہو سکتا ہے۔ مزید یہ کہ کئی جوہری جین کی تبدیلیاں مائٹوکونڈریل سانس کی زنجیر اور اس کے اجزاء کو براہ راست متاثر کر سکتی ہیں۔ کمپلیکس I (NDuFS1, NDuFS2, NDUFS3)، پیچیدہ IV(SURF1, SCO1, SCO2, COX10, COX15), پیچیدہ V(ATP12, TMEM70), mitochondrial Translation (TACO1, EFG1)، اور cardiolipins کی جینز میں تبدیلیاں ) کارڈیو مایوپیتھی سے وابستہ ہیں [59]۔ مزید برآں، انٹرمیوفائبرلر مائٹوکونڈریا لمبے اور گھنے آرگنیلس اور کنٹریکٹائل مائیوفلامینٹس کے ایک منظم نیٹ ورک کی نمائندگی کرتا ہے۔ دل کی ناکامی میں، انٹرمیوفائبرلر مائٹوکونڈریا اور سارکوپلاسمک ریٹیکولر کے درمیان جسمانی اور کیمیائی تعاملات میں خلل کارڈیو مایوسائٹ کے سنکچن کو کم کرتا ہے اور خلیوں کی موت کا باعث بنتا ہے[63]۔ مزید برآں، دل کی ناکامی کو مائٹوکونڈریل کیلشیم اوورلوڈ، زیادہ ROS ریلیز، اور ATP کی پیداوار میں کمی [64] کی طرف سے خصوصیت دی جا سکتی ہے۔ دل کی ناکامی کے دوران، کیلشیم کا اوورلوڈ عام طور پر مائٹوکونڈریل فیشن اور ناکارہ ہونے میں اضافہ کرتا ہے۔ اس کے بعد، یہ عمل دل کی سرگرمی میں کمی کا باعث بنتے ہیں جس کی خصوصیت بائیں ویںٹرکل کو بھرنے اور جسم کی ضروریات کے مطابق خون نکالنے کی کم صلاحیت سے ہوتی ہے۔ دل کی یہ میٹابولک مانگ دل کی دھڑکن میں تبدیلی، مایوکارڈیل انوٹروپک حالت، اور مایوکارڈیل دیوار کے تناؤ سے منسلک ہوسکتی ہے جو کہ آخر میں دل کی چوٹ کو فروغ دیتی ہے۔ کیلشیم کا جمع مائٹوکونڈریل انرجیٹکس (اے ٹی پی پروڈکشن) میں کمی سے بھی وابستہ ہے جو سیل کو نقصان پہنچانے والے ROS اور اپوپٹوسس انڈکشن [65] کی نسل سے وابستہ ETC اور OXPHOS میں منفی تبدیلیوں کا باعث بنتا ہے۔ مزید برآں، کارڈیولپین ETC کی سرگرمی کے لیے درکار اندرونی مائٹوکونڈریل جھلی میں ایک کلیدی مائٹوکونڈریل فاسفولیپڈ ہے۔ کارڈیولپین کا نقصان کارڈیو لیپن پیرو آکسیڈیشن اور سائٹوکوم سی کی رہائی میں خلل سے منسلک ROS کی پیداوار کا سبب بنتا ہے جس سے کارڈیو مایوسائٹ اپوپٹوس ہوتا ہے۔ دل کی ناکامی میں، یہ شیطانی چکر مائٹوکونڈریل dysfunction اور اس کے نتیجے میں کارڈیو مایوسائٹ موت کا باعث بنتا ہے [66]۔
2.3۔ نیوروڈیجنریشن میں مائٹوکونڈریوپیتھیس
انتہائی پولرائزڈ نیوران [67,68] میں قطبیت کو برقرار رکھنے کے لیے نارمل مائٹوکونڈریل ڈائنامکس اہم ہیں۔ دماغی عوارض (نیوروڈیجنریشن) اور چوٹ (نیوروٹوکسیسیٹی اور اسکیمیا) میں نیورونل سیل کی موت مائٹوکونڈریل ہومیوسٹاسس اور/یا فنکشن میں مختلف تبدیلیوں سے منسلک ہے جس میں ٹریفک، کوالٹی کنٹرول، ٹرن اوور، بائیو انرجیٹکس، الیکٹران ٹرانسپورٹ، اور سگنلنگ [69] شامل ہیں۔ نیوران اپنی توانائی کے تقاضوں کو پورا کرنے کے لیے OXPHOS پر زیادہ انحصار کرتے ہیں دوسرے سیل اقسام کے مقابلے [70]۔ نیوروڈیجینریٹو عوارض بھی ایم ٹی ڈی این اے اتپریورتنوں کے بتدریج جمع ہونے کی خصوصیت رکھتے ہیں جو ممکنہ طور پر ای ٹی سی اور اے ٹی پی کی پیداواری کارکردگی کو کم کرسکتے ہیں اور آر او ایس کی پیداوار کو بڑھا سکتے ہیں [71]۔ ایک اعلی ROS کی سطح ایک "شیطانی دائرے" میں مزید mtDNA اتپریورتنوں کا سبب بن سکتی ہے جو خلیوں کی موت کا باعث بنتی ہے [72]۔ مزید برآں، مائکروٹوبول سے وابستہ پروٹین تاؤ (تاؤ) کی اسامانیتاوں کو مختلف نیوروڈیجینریٹو عوارض میں دیکھا گیا، بشمول الزائمر کی بیماری (AD)، پارکنسنز کی بیماری (PD)، اور پک کی بیماری [73]۔ مائٹوکونڈریل dysfunction AD میں تاؤ پیتھالوجی کے ساتھ قریبی تعلق ہے؛ ہائپر فاسفوریلیٹڈ اور ایگریگیٹڈ تاؤ کے زیادہ اظہار سے محوری نقل و حمل کو نقصان پہنچانے اور مائٹوکونڈریا کی غیر معمولی تقسیم کا سبب بننے کا مشورہ دیا جاتا ہے [74]۔
Mitochondrial dysfunction اور oxidative stress AD اور PD میں حصہ ڈالتے ہیں، جو عمر سے متعلق دو سب سے عام نیوروڈیجینریٹو بیماریاں ہیں [71]۔ AD، عمر رسیدہ ڈیمنشیا کی ایک شکل، عمر بڑھنے کے دوران خراب شدہ مائٹوکونڈریا کے جمع ہونے کی خصوصیت ہے۔ AD کے مریضوں کے دماغی پرانتستا میں amyloid-peptide(A) تختیوں کا ایکسٹرا سیلولر جمع اور نیوروفائبریلری ٹینگلز (NFIs) کی انٹرا سیلولر تشکیل [75]۔ AD میں، ہائپر فاسفوریلیٹڈ pTau کے ساتھ A کے oligomers Synaptic فنکشن اور علمی خرابی کا سبب بنتے ہیں [76,77]۔ متعدد تغیرات مائٹوکونڈریل فنکشن کے ساتھ قریب سے وابستہ ہیں، جن میں جینز انکوڈنگ -amyloid precursor protein (APP)، presenilin 1(PSEN1) اور 2(PSEN2)، اور apolipoprotein E(APOE4)، AD کی ترقی کا باعث بنتے ہیں۔ مائٹوکونڈریل اے پی پی کی مختلف غلط فہمیاں یا حذف ہونے والی تبدیلیاں AD [73] کی وراثتی شکل کا سبب بنتی ہیں۔ اے پی پی اتپریورتنوں کے علاوہ، PSENI اور PSEN2 میں اتپریورتنوں کو ابتدائی طور پر خاندانی AD [78] میں دیکھا جاتا ہے۔ مزید برآں، AD روگجنن میں APOE4 کا تعاون APOE4-A مجموعے اور کلیئرنس کی ثالثی تبدیلیوں سے متعلق ہے۔ دیر سے شروع ہونے والے چھٹپٹ AD [79] کے لئے APOE4 اتپریورتن ایک اہم جینیاتی خطرے کے عوامل میں سے ایک ہے۔
مزید برآں، PD کے پیتھولوجیکل نشانات میں سبسٹینٹیا نگرا میں ڈوپیمینرجک نیورونز کا نقصان اور انٹرا سائٹوپلاسمک انکلوژنز میں غلط فولڈ سائنوکلین (c-syn) کی موجودگی شامل ہے جسے لیوی باڈیز [80] کہا جاتا ہے۔ PD مختلف mitochondrial dysfunctions سے پیدا ہوتا ہے، بشمول bioenergetic اور transscriptional نقائص، اور حرکیات (فیوژن یا فیوژن)، سائز، مورفولوجی، اسمگلنگ، نقل و حمل اور نقل و حرکت میں تبدیلی۔ بلاشبہ، ایم ٹی ڈی این اے، نیوکلیئر ڈی این اے، اور مائٹوکونڈریل پروٹین میں تغیرات کو PD [81] میں اچھی طرح سے بیان کیا گیا ہے۔ لہذا، E3 ubiquitin ligase (Parkin)، c-syn، ایک پارکن سے وابستہ پروٹین جو آکسیڈیٹیو اسٹریس (DJ1)، ubiquitin carboxy-terminal hydrolase L1 (UCHL1)، auxilin (DNAJC6)، پوٹیٹیو سیرین تھرونائن کناز میں تبدیلیاں یا خلل ڈالتا ہے۔ (PINKT)، synaptojanin1 (SYN1)، serine peptidase 2 (HTRA2)، اور endophilin A1 (SH3GL2) کئی مائٹوکونڈریل افعال میں خلل ڈالتے ہیں اور PD کی نشوونما کا سبب بن سکتے ہیں [12]۔

3. Flavonoids کی درجہ بندی اور افعال
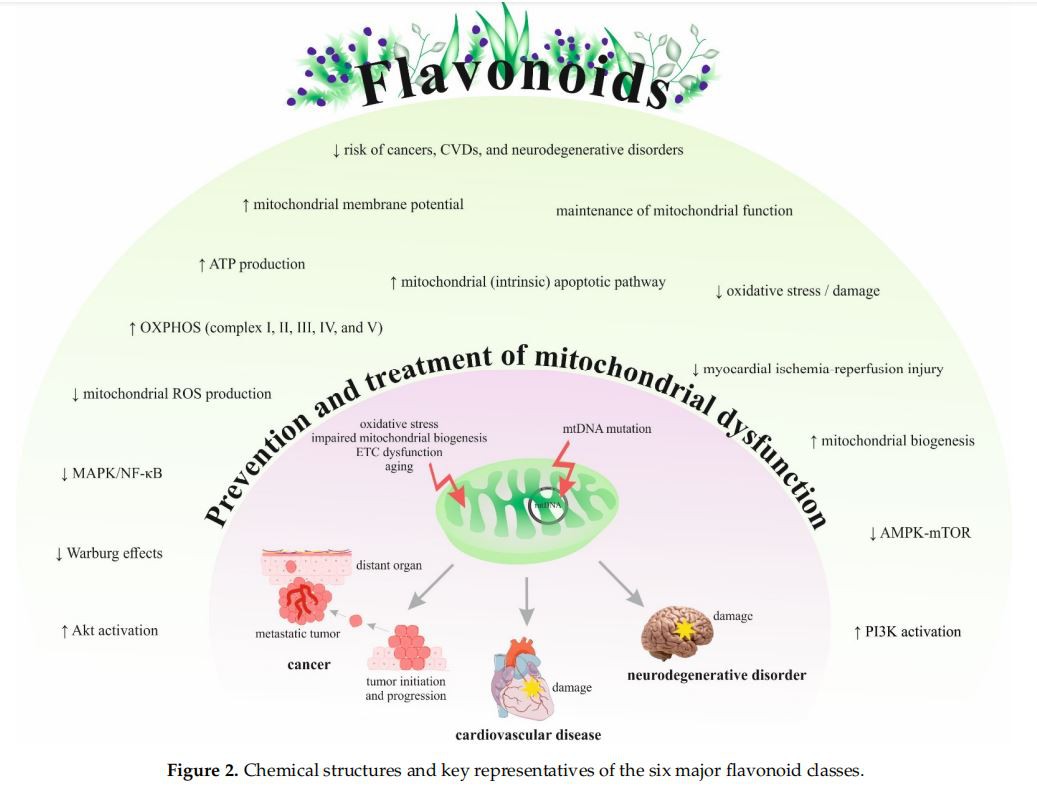
Flavonoids قدرتی مادوں کے ایک اہم طبقے کی نمائندگی کرتے ہیں۔ تمام فلیوونائڈز پودوں میں بائیو ایکٹیو ثانوی میٹابولائٹس کے طور پر ترکیب کیے جاتے ہیں اور اس میں ایک بنیادی فلاوان کنکال ہوتا ہے جو ایک 15-کاربن فینائل پروپینائڈ چین (C6-C3-C6 سسٹم) پر مشتمل ہوتا ہے جس میں ایک خصوصیت والی پولی فینولک ساخت ہوتی ہے۔ دو فینائل رِنگز اور ایک ہیٹروسائکلک پائران رنگ [82,83]۔ Flavonoids کو چھ بڑے گروپوں میں تقسیم کیا جا سکتا ہے: isoflavonoids، flavanones، flavanols، flavanols، flavones، اور anthocyanidins [84]۔ flavonoids کی اضافی معمولی کلاسوں میں chalcones، dihydrochalcones، اور aurones کو معمولی flavonoids میں درجہ بندی کیا جاتا ہے [85,86]۔ مزید برآں، فلیوونائڈز پودوں پر مبنی کھانوں میں وافر مقدار میں ہوتے ہیں اور اس طرح پھلوں، سبزیوں، گری دار میوے، بیج، اناج، چھال، جڑوں، تنوں، پھولوں، چائے اور شراب کے ذریعے استعمال ہوتے ہیں [84]۔ عام کیمیائی ڈھانچے [83] اور چھ بڑے flavonoid کلاسوں [87,88] کے کلیدی نمائندوں کو شکل 2 میں پیش کیا گیا ہے۔
فلاوونائڈز میں بہت سے فائدہ مند خصوصیات ہیں، جیسے کہ اینٹی آکسیڈینٹ، فری ریڈیکل اسکیوینجنگ، ہیپاٹوپروٹیکٹو، کارڈیو پروٹیکٹو، اینٹی انفلامیٹری، امیونو موڈولیٹری، اینٹی اینجیوجینک، اینٹی وائرل، کینسر مخالف سرگرمیاں، اور اینٹی ڈپریسنٹ جیسے اثرات [82,89-91]۔ مختلف flavonoids (vitexin، اور baicalin) اور دیگر فائٹو کیمیکل مرکبات جیسے curcumin (diarylheptanoid)، lycopene (carotene)، اور ginsenoside (triterpenes)، اسکیمک سے متاثرہ چوٹ کے خلاف نیورو پروٹیکٹو اثرات رکھتے ہیں [92]۔ مزید برآں، flavonoids کئی کلیدی مائٹوکونڈریل انزیمیٹک راستوں کو ماڈیول کر سکتے ہیں [93]۔ فلیوونائڈز کے کیمیائی ڈھانچے سے وابستہ ریڈوکس پوٹینشل ان مرکبات کو تھرموڈینامک طور پر ROS کو ختم کرنے کی اجازت دیتے ہیں، بشمول ہائیڈروکسیل، سپر آکسائیڈ، الکوکسل، الکائل پیروکسائل، اور نائٹرک آکسائیڈ ریڈیکلز [94]۔ دوسری طرف، ریڈوکس کے آکسائڈائزڈ ری ایکٹو بائی پراڈکٹس اور فلیوونائڈز کے سکیوینجنگ میکانزم ان مرکبات کو کیمیائی طور پر غیر مستحکم کرتے ہیں [95]۔ خاص طور پر، flavonoids کی ریڈوکس خصوصیات سیلولر حالات، خوراک، علاج کے وقت، تجرباتی ماڈل، ٹیومرجینک حالت، اور دیگر عوامل کے ساتھ مختلف ہوتی ہیں۔ مخصوص سیلولر حالات جیسے ماحولیاتی عوامل یا تناؤ کی موجودگی کے تحت، اینٹی آکسیڈینٹ پرو آکسیڈینٹس کے طور پر بھی کام کر سکتے ہیں۔ فلاوونائڈز کی پرو آکسیڈینٹ سرگرمی، مثلاً، لیوٹولن اور فِسیٹِن، کو سپر آکسائیڈ اینونز [96,97] پیدا کرنے کے لیے ٹرانزیشن میٹلز کے ذریعے اتپریرک آٹو آکسیڈیشن سے گزرنے کی صلاحیت سے خصوصیت دی جا سکتی ہے۔ پراکسیڈینٹ کی حیثیت کے تعین کے لیے مختلف ریڈکٹنٹ آکسیڈینٹ مارکروں کا جائزہ لینا ضروری ہے جیسے گلوٹاتھیون (GSH) سے GSSG، NADPH سے NAPD-، اور NADH سے NAD-[98]۔ فلیوونائڈز کی پراکسیڈینٹ خصوصیات مختلف بائیو مالیکیولز جیسے لپڈز، پروٹینز اور ڈی این اے [99,100] کے ساتھ رد عمل کے ذریعے آکسیڈیٹیو نقصان کا سبب بن سکتی ہیں۔
فلاوونائڈز عام طور پر ان کی ناقص پانی میں حل پذیری کی وجہ سے کم زبانی حیاتیاتی دستیابی کا مظاہرہ کرتے ہیں۔ ان کے ذرائع کی ساخت ان کی جیو دستیابی کو بھی متاثر کر سکتی ہے۔ لہذا، گٹ مائکروبیوم flavonoids کے جذب اور میٹابولزم کے لئے اہم ہے [101]۔ Anthocyanidins اور pro-anthocyanidins کی حیاتیاتی دستیابی سب سے کم ہے، جبکہ quercetin glucosides، catechin، flavanones، isoflavones، اور gallic acid سب سے زیادہ ہے [102]۔ یہ وہ مسئلہ ہے جس پر بائیو ٹکنالوجی کے نقطہ نظر سے غور کیا جانا چاہیے تاکہ ان کی جیو دستیابی میں اضافہ ہو اور طبی عمل درآمد میں آسانی ہو۔
Flavonoids 3 PM کے فریم ورک میں ایک قابل قدر شراکت فراہم کرتے ہیں۔ 3 PM کا کردار لاگت سے مؤثر ہدفی روک تھام اور طبی خدمات کو ذاتی بنانے کے ذریعے پیش گوئی کرنے والے تجزیاتی نقطہ نظر کو متعارف کرانا ہے۔ پیش گوئیاں اور ابتدائی تشخیص، زیادہ خطرہ والے افراد کو نشانہ بنانا، مریضوں کی انفرادی پروفائلنگ، اور مریض کی سطح بندی مختلف بیماریوں کے علاج کی حکمت عملیوں کو نمایاں طور پر بہتر بنا سکتی ہے [12]۔ اوپر بیان کردہ حدود کے باوجود، فلیوونائڈز طویل مدتی انتظامیہ کے دوران کم سے کم ضمنی اثرات کے ساتھ ماحول دوست اور سستی مادے کی نمائندگی کرتے ہیں۔ flavonoids کے صحت کے لیے فائدہ مند اثرات 3 PM کے تصورات کے لیے امید افزا ہیں جن میں پیشن گوئی کے نقطہ نظر، ہدف کی روک تھام، اور طبی خدمات کو ذاتی بنانا شامل ہیں، جو مثبت طور پر روک تھام اور علاج کی حکمت عملیوں پر اثر انداز ہو سکتے ہیں، مثلاً، flavonoids کے کینسر مخالف اثرات جو میٹاسٹیسیس کے آغاز کو روک سکتے ہیں اور زیادہ خطرہ والے افراد میں ان کا پھیلاؤ [86]۔





