وائرل انفیکشن مائٹوکونڈریل فنکشن کو ماڈیول کرتا ہے۔
Sep 07, 2023
خلاصہ: مائٹوکونڈریا ایک اہم عضو ہیں جو میٹابولزم میں شامل ہیں اور یوکرائیوٹک خلیوں میں سیل ڈیتھ پروگرامڈ ہیں۔ اس کے علاوہ، مائٹوکونڈریا کا وائرس کے خلاف میزبان خلیوں کی فطری قوت مدافعت سے بھی گہرا تعلق ہے۔ مائٹوکونڈریل مورفولوجی اور فنکشن کی غیر معمولی بیماری مختلف بیماریوں کا باعث بن سکتی ہے۔ مطالعے کی ایک بڑی تعداد نے پایا ہے کہ وائرل انفیکشن کی ایک قسم مائٹوکونڈریل حرکیات کو تبدیل کر سکتی ہے، مائٹوکونڈریا کی حوصلہ افزائی سیل کی موت میں ثالثی کر سکتی ہے، اور انٹرا سیلولر بقا کو برقرار رکھنے کے لیے مائٹوکونڈریل میٹابولک حیثیت اور سیلولر پیدائشی مدافعتی ردعمل کو تبدیل کر سکتی ہے۔ دریں اثنا، مائٹوکونڈریا وائرل انفیکشن کے دوران ایک اینٹی وائرل کردار بھی ادا کر سکتا ہے، اس طرح میزبان کی حفاظت کرتا ہے۔ لہذا، مائٹوکونڈریا میزبان اور وائرس کے درمیان تعامل میں اہم کردار ادا کرتا ہے۔ اس کے ساتھ، ہم خلاصہ کرتے ہیں کہ وائرل انفیکشن کس طرح مائٹوکونڈریل مورفولوجی اور فنکشن کو تبدیل کرکے مائکروبیل روگجنن کو متاثر کرتے ہیں اور کس طرح وائرس میزبان کے مدافعتی ردعمل سے بچ جاتے ہیں۔
مطلوبہ الفاظ: مائٹوکونڈریل فیوژن اور فیوژن؛ وائرس کا انفیکشن؛ apoptosis؛ پیدائشی استثنیٰ کی میزبانی کریں۔

cistanche پلانٹ میں مدافعتی نظام میں اضافہ
1. مائٹوکونڈریا کی فزیولوجیکل مورفولوجی
مائٹوکونڈریا کی ابتدا ایک قدیم بیکٹیریل اینڈوسیمبیونٹ سے ہوئی ہے، اور تقریباً تمام خلیوں میں پائے جانے والے اہم عضو ہیں۔ تقریبا 130 سالوں میں جب سے مائٹوکونڈریا پہلی بار رپورٹ ہوا تھا، نئے افعال دریافت ہوئے ہیں۔ مائٹوکونڈریا مائٹوکونڈریل نیٹ ورک کا متحرک توازن برقرار رکھتا ہے فیوژن اور فیوژن کے ذریعے ڈائنامین سے متعلق GTPases کے ایک وقف سیٹ کے ذریعے ثالثی کرتا ہے، خلیات کے لیے توانائی فراہم کرتا ہے، اور آٹوفیجی، کیلشیم ہومیوسٹاسس، فطری قوت مدافعت، سگنل کی منتقلی، اور اپوپٹوسس جیسے عمل کو منظم کرتا ہے۔ ] مائٹوکونڈریا سیل کے اندر ایک انتہائی متحرک عمل میں ہے، مائٹوکونڈریا کی شکل کو کنٹرول کرنے کے لیے فیوژن اور فیوژن سائیکل سے گزر رہا ہے۔ فزی پیاز (Fzo) پہلا پروٹین ہے جو ڈروسوفلا اسپرمیٹوجنیسس کے دوران مائٹوکونڈریل فیوژن میں ثالثی کے لیے دریافت کیا گیا ہے، اور Fzo جین میں تغیرات مائٹوکونڈریل فیوژن کی خرابی اور ڈروسوفلا سپرم سیلز میں غیر معمولی جمع ہونے کا سبب بن سکتے ہیں [2]۔ ممالیہ جانوروں میں، پروٹین جو مائٹوکونڈریل فیوژن میں ثالثی کرتے ہیں ان میں بنیادی طور پر Mfn1 (Mitofusin1)، Mfn2 (Mitofusin2)، اور OPA1 (Optic atrophy 1) [3–5] شامل ہیں۔ Mfns ہیپٹاد ریپیٹ ریجنز (HR2) پر مشتمل ہے، اور Mfn1 اور Mfn2، جو بیرونی مائٹوکونڈریل جھلی (OMM) پر واقع ہیں، HR2 ڈھانچے کے اولیگومرائزیشن کے ذریعے Mfn1/Mfn2 homodimers یا Mfn1/Mfn2 heterodimers بنانے کے لیے تعامل کرتے ہیں، اس طرح ٹرانسپلانٹ کے مرحلے کو فروغ دیتے ہیں۔ ملحقہ OMM [6,7]، اور اس میں GTP ہائیڈرولیسس شامل ہے، جو آخر کار OMM [8,9] کے فیوژن کی طرف جاتا ہے۔ OPA1، ایک متحرک طور پر متعلقہ GTPase IMM میں مقامی ہے، IMM فیوژن میں حصہ لیتا ہے۔ OPA1 پروٹین کو انٹرمیمبرن اسپیس میں مختلف ٹکڑوں میں ہائیڈولائز کیا گیا تھا: ایک طویل ذیلی قسم L-OPA1 ہے جو مائٹوکونڈریل فیوژن سے وابستہ ہے، اور دوسرا مختصر ذیلی قسم S-OPA1 [10,11] ہے۔ L-OPA1 اپنے GTPase ڈومین اور اس کے ملحقہ mitochondrial membrane cardiolipid (CL) کے درمیان heteromorphic تعامل کے ذریعے منتخب مائٹوکونڈریل فیوژن کو حاصل کرتا ہے۔ فیوژن میں ثالثی کرنے والے پروٹین (MFN1، MFN2، اور OPA1) کا نقصان مائٹوکونڈریل مورفولوجی میں تبدیلیوں کا سبب بن سکتا ہے، جس کے نتیجے میں مائٹوکونڈریل فریگمنٹیشن ہوتا ہے۔ مائٹوکونڈریل فیوژن ایک ضروری سیلولر عمل ہے جو مائٹوکونڈریل ٹکڑوں کو ملانے میں سہولت فراہم کرتا ہے اور مائٹوکونڈریل ڈی این اے، پروٹین اور میٹابولائٹس کے تبادلے میں ثالثی کرتا ہے۔ جین ناک آؤٹ اور آر این اے مداخلت کی تکنیکوں کے ذریعہ مائٹوکونڈریل کنوننس پروٹین کو حذف کردیا گیا تھا ، جس کے نتیجے میں مائٹوکونڈریل فریگمنٹیشن [3,5] ہوتا ہے۔ مائٹوکونڈریا تباہ شدہ مائٹوکونڈریا کو "مائٹوکونڈریل فِشن" کے ذریعے بھی توڑ سکتا ہے، انہیں چھوٹے ٹکڑوں میں توڑ سکتا ہے۔ ممالیہ کے خلیوں میں، Drp1 ایک اہم پروٹین ہے جو مائٹوکونڈریل فیشن میں ثالثی کرتا ہے۔ Drp1 کو چالو کرنے کے بعد، اسے سائٹوسول سے OMM میں بھرتی کیا جاتا ہے، جہاں oligomerization ہوتا ہے۔ Drp1 OMM کے قطر کے اندر حلقے اور سرپل بناتا ہے اور GTP کو اس کی GTP-اینزائم سرگرمی کے لحاظ سے ہائیڈولائز کرتا ہے، جس کے نتیجے میں جھلیوں کی تنگی اور کٹائی ہوتی ہے [12,13]۔ Drp1 کی نقل و حمل اور کام کو دو کلیدی سیریز میں فاسفوریلیشن کے مخالف اثرات سے تیزی سے منظم کیا جاتا ہے۔ عام طور پر، سیرین 616 کا فاسفوریلیشن Drp1 کی سرگرمی کو بڑھاتا ہے اور اس کے مائٹوکونڈریل ایگریگیشن کے ہدف کو فروغ دیتا ہے، جبکہ سیرین 637 میں فاسفوریلیشن Drp1 کی سرگرمی کو کم کر دیتا ہے، اسے سائٹوپلازم میں رکھتا ہے [14]۔ مثال کے طور پر، RIP1 Drp1 کی Ser616 باقیات کو فاسفوریلیٹ کرتا ہے، اس طرح مائٹوکونڈریل فِشن کو آمادہ کرتا ہے اور مائٹو فیگی کے ذریعے تباہ شدہ مائٹوکونڈریا کو ختم کرتا ہے، جب خلیے توانائی کے دباؤ کی حالت میں ہوتے ہیں [15]۔ Drp1 کے Ser637 پر فاسفوریلیشن جی ای ڈی ڈومین کے ساتھ جی ٹی پی بائنڈنگ/مڈل ڈومینز کے تعامل کو روکتا ہے، اس طرح جی ٹی پیز کی سرگرمی کو کم کرتا ہے اور Drp1 فنکشن اور مائٹوکونڈریل مورفولوجی کو تبدیل کرتا ہے [16]۔ Drp1 کو اپنا کام انجام دینے کے لیے مختلف لوازمات کے پروٹین کی ضرورت ہوتی ہے۔ اس وقت، mitochondrial fission factor (mitochondrial fission factor, Mff)، mitochondrial fission protein 1 (mitochondrial fission protein 1, Fis1)، mitochondrial dynamin 49 (mitochondrial dynamics proteins of 49 kDa، Mi D49 mitochondrial dynamics proteins)، اور 1550 کے ڈی اے کے مائٹوکونڈریل ڈائنامکس پروٹینز۔ کے 51 kDa، MiD51) مائٹوکونڈریا پر واقع Drp1 کے لیے ligands کے طور پر کام کرتے پائے گئے ہیں، جو Drp1 کو مائٹوکونڈریا میں بھرتی کرتے ہیں اور mitochondrial fission [17] کو منظم کرتے ہیں۔ Fis1، خمیر کے خلیوں میں واحد Dnm1 رسیپٹر، ممالیہ کے خلیوں میں مائٹوکونڈریا میں Drp1 کو بھرتی کرنے کے لیے متنازعہ ہے۔ مثال کے طور پر، Fis1 اور Drp1 ممالیہ جانوروں کے خلیوں میں تعامل کرتے ہیں، اور Fis1 کی سطح میں اضافہ مائٹوکونڈریل فِشن کو فروغ دے گا [18]۔ تاہم، بڑی آنت کے کینسر کے خلیوں میں Fis1 کو حذف کرنے سے پتہ چلتا ہے کہ یہ مائٹوکونڈریل ڈویژن [19] کے لیے ضروری نہیں ہے۔ ایک حالیہ تحقیق سے پتا چلا ہے کہ انسانی Fis1 Mfn1، Mfn2، اور OPA1 کے پابند ہو کر مائٹوکونڈریل فیوژن میکانزم کو روکتا ہے، یہ تجویز کرتا ہے کہ Drp1 انسانی Fis1 فنکشن کے لیے قابل استعمال ہے [20]۔ Mff پروٹین بھی Drp1 کا ایک ریسیپٹر مالیکیول ہے، یہ Drp1 کے ساتھ امینو ٹرمینل سائٹوپلاسمک ریجن کے ذریعے تعامل کرتا ہے اور OMM پر یکساں طور پر تقسیم ہوتا ہے، بنیادی طور پر Drp1 [19] جیسی جگہوں پر۔ Mff کا زیادہ اظہار مائٹوکونڈریا میں Drp1 کی بھرتی کو فروغ دے سکتا ہے جبکہ Mff اظہار کو خاموش کرنے سے مائٹوکونڈریل فیوژن کو فروغ مل سکتا ہے۔ اس کے علاوہ، مائٹوکونڈریل ڈائنامکس پروٹین (MiDs) fifis1 اور Drp1 کی کمی والے خلیوں میں mitochondrial fission میں شامل ہیں۔ جب ایم آئی ڈی زیادہ متاثر ہوتے ہیں، تو وہ مائٹوکونڈریا میں ثالثی کرنے کے لیے غیر فعال S637 فاسفوریلیٹڈ Drp1 کی ایک بڑی تعداد کو مائٹوکونڈریا میں بھرتی کرتے ہیں [21,22]۔ مائٹوکونڈریا سیلولر سرگرمیوں کی ایک سیریز میں شامل ہے جیسے سیل میٹابولزم، پروگرام شدہ سیل کی موت اور فطری قوت مدافعت، اور وائرل انفیکشن کے میزبان ردعمل۔ مزید برآں، طویل مدتی ارتقائی عمل میں، وائرسز نے مائٹوکونڈریا کو نشانہ بنا کر اپنی انٹرا سیلولر بقا کو متاثر کرنے کے لیے ایک راستہ تیار کیا ہے، اور مائٹوکونڈریا کی وجہ سے سیل کی موت میں ثالثی کرکے، وہ میزبان قوت مدافعت کو پھیلا سکتے ہیں یا اس سے بچ سکتے ہیں۔ اس جائزے میں، ہم دریافت کرتے ہیں کہ وائرس کیسے مائٹوکونڈریا میں ہیرا پھیری کرتے ہیں اور یہ ہیرا پھیری مائکروبیل روگجنن کو کیسے متاثر کرتی ہے۔

Cistanche جڑی بوٹیوں کے اثرات - Antitumor
2. وائرل انفیکشن مائٹوکونڈریل ڈائنامکس میں خلل ڈالتا ہے۔
مختلف قسم کے وائرل انفیکشن مائٹوکونڈریا کے متحرک توازن کو تباہ کر کے مائٹوکونڈریل آٹوفجی کو آمادہ کر سکتے ہیں، جو خود وائرل انفیکشن کے لیے موزوں ہے۔ ہیپاٹائٹس سی وائرس (HCV) کے مریضوں میں مائٹوکونڈریل مورفولوجیکل تبدیلیوں کی ابتدائی دریافت کے بعد سے، زیادہ سے زیادہ مطالعات نے HCV انفیکشن کی وجہ سے مائٹوکونڈریل فنکشن میں ہونے والی تبدیلیوں پر توجہ مرکوز کی ہے، جو کہ ایک مثبت اسٹرینڈ RNA وائرس ہے [23]۔ HCV کور پروٹین کو نشانہ بنایا جا سکتا ہے اور OMM پر واقع ہو سکتا ہے، جس کے نتیجے میں الیکٹران ٹرانسپورٹ کمپلیکس I میں کمی، مائٹوکونڈریل الیکٹران ٹرانسپورٹ کی روک تھام، اور رد عمل آکسیجن پرجاتیوں (ROS) [24,25] کی پیداوار میں اضافہ ہوتا ہے۔ HCV کور، E1، اور NS3 پروٹین کے ذریعے ROS کی پیداوار کو بھی آمادہ کرتا ہے، جو مائٹوکونڈریل پارگمیٹی ٹرانزیشن کو متحرک کرتا ہے، جس سے DNA کو نقصان ہوتا ہے اور STAT3 ایکٹیویشن [26]۔ Ca2+ اور ROS کی وجہ سے مائٹوکونڈریل پارگمیتا کی حد کو کم کرنا ہیپاٹائٹس سی وائرس کے انفیکشن کی ایک خصوصیت ہے۔ یہ مائٹوکونڈریا [27] کے ساتھ ایچ سی وی کور پروٹین کے تعامل کا براہ راست نتیجہ ہے۔ ایچ سی وی انفیکشن وائرل ثابت قدمی کو فروغ دینے کے لیے مائٹوکونڈریل فِشن اور مائٹوفگی کو فروغ دے کر مائٹوکونڈریل ڈائنامکس کو بھی متاثر کرتا ہے۔ HCV Drp1 (Ser616) کے فاسفوریلیشن کو اکساتا ہے اور اسے مائٹوکونڈریا میں منتقل کرتا ہے تاکہ مائٹوکونڈریل فِشن میں ثالثی کر سکے، اس طرح مائٹوفجی [28] کا سبب بنتا ہے۔ HCV کی حوصلہ افزائی mitochondrial fission اور mitophagy کی مداخلت گلائکولائسز اور ATP کی پیداوار کو کم کرنے کے ساتھ ساتھ انٹرفیرون کی ترکیب کو بڑھا سکتی ہے، اس طرح وائرل رطوبت کو روکتی ہے [28]۔ ایک اور تحقیق سے پتہ چلتا ہے کہ HCV سے حوصلہ افزائی شدہ mitochondrial fission نہ صرف DRP1 پروٹین پر منحصر ہے، بلکہ HCV NS5A پروٹین فاسفیٹائیڈیلینوسیٹول 4-کناز III کے ساتھ بھی تعامل کر سکتا ہے، جو مائٹوکونڈریل فریگمنٹیشن [29] کو آمادہ کرتا ہے۔ HCV پارکن اور PINK1 کے اظہار کی حوصلہ افزائی کرتا ہے اور مائٹو فیجی میں ثالثی کے لیے پارکن کی نقل مکانی کو مائٹوکونڈریا میں متحرک کرتا ہے۔ پارکن اور PINK1 کو خاموش کر کے مائٹوفگی کی روک تھام مائٹوکونڈریل کمپلیکس I انزائم کی سرگرمی کو جزوی طور پر بچا سکتی ہے اور HCV کی نقل کو روک سکتی ہے [28]۔ دلچسپ بات یہ ہے کہ HCV کور پروٹین پارکن کے ساتھ تعامل کرتا ہے، پارکن کی نقل مکانی کو مائٹوکونڈریا میں روکتا ہے، جس کے نتیجے میں مائٹوکونڈریل آٹوفاگوسومز کی تشکیل اور آٹوفجی انحطاط کی ناکامی ہوتی ہے [30]۔ کلاسیکی سوائن فیور وائرس (CSFV) اور ڈینگی وائرس (DENV) وائرس کے اسی خاندان سے تعلق رکھتے ہیں جیسا کہ HCV کرتا ہے، اور انفیکشن مائٹوکونڈریا کے فنکشن [31–35] کو متاثر کر کے خود کی نقل تیار کرنے میں بھی سہولت فراہم کر سکتا ہے۔ CSFV انفیکشن MNF2 کو ہر جگہ اور انحطاط کا سبب بنتا ہے اور پارکن اور PINK1 اور mitochondrial translocation کے اظہار کو متحرک کرتا ہے، جس سے mitochondrial fission اور mitophagy میں اضافہ ہوتا ہے۔ ڈی آر پی 1 اور پارکن کو خاموش کرنے کے نتیجے میں سی ایس ایف وی کی نقل میں کمی واقع ہوئی [31]۔ DENV پروٹین NS4B اور NS3 Drp1-متحرک مائٹوکونڈریل فِشن کو روک کر مائٹوکونڈریل ڈائنامکس میں عدم توازن پیدا کرتے ہیں، جو DENV کی نقل کے لیے موزوں ہے۔ اس کے علاوہ، DENV کا NS4B پروٹین DRP1 کو غیر فعال کر سکتا ہے اور مائٹوکونڈریل لمبائی میں ثالثی کر سکتا ہے [34]۔ مائٹوکونڈریل ایکسٹینشن مائٹوکونڈریا کو کنولوٹیڈ میمبرینز (سی ایم) کے ساتھ رابطے میں لاتا ہے اور مائٹوکونڈریل سے وابستہ جھلی (ایم اے ایم) پر مائٹوکونڈریا-اینڈوپلاسمک ریٹیکولم بائنڈنگ سائٹ کی سالمیت کو تباہ کرتا ہے، جس کے نتیجے میں RLR سگنل کی نقل و حمل کی ناکامی اور مداخلت کی پیداوار میں کمی واقع ہوتی ہے۔ تاہم، ایک اور تحقیق سے پتا چلا ہے کہ DENV MFN1 اور MFN2 کے NS2B3 پروٹین کلیویج کے ذریعے مائٹوکونڈریل فیوژن کو بھی روک سکتا ہے، RLR سگنل کی نقل و حمل کو روکتا ہے اور مائٹوکونڈریل جھلی کی صلاحیت کو تباہ کر سکتا ہے، اس طرح DENV انفیکشن میں اضافہ ہوتا ہے [35]۔ یہ بھی بتایا گیا ہے کہ ہیپاٹائٹس بی وائرس (HBV)، ایک جزوی طور پر ڈبل پھنسے ہوئے DNA وائرس جو Hepatoviridae خاندان سے تعلق رکھتا ہے، mitochondrial حرکیات کو تبدیل کرکے جگر کے خلیوں میں mitochondrial نقصان میں ثالثی کر سکتا ہے، اس طرح جگر کی بیماریوں کا باعث بنتا ہے۔ بہت سے مطالعات میں بتایا گیا ہے کہ HBV HBx پروٹین مائٹوکونڈریا کو نشانہ بنا سکتا ہے اور OMM، IMM، یا میٹرکس میں واقع ہو سکتا ہے۔ مطالعات سے پتہ چلتا ہے کہ مارچ 5، ایک mitochondrial E3 ubiquitin ligase، polyubiquitination کے ذریعے mitochondria پر جمع HBx کو کم کر سکتا ہے اور Drp1، Fis1، اور Mfn1 کے ہر جگہ استعمال ہونے کے ذریعے مائٹوکونڈریل حرکیات کو منظم کر سکتا ہے، اس طرح HB کو منفی طور پر [36] کو منظم کرتا ہے۔ HBx نے پارکن کو PINK1 اظہار کو ریگولیٹ کرکے depolarized/غیر فعال مائٹوکونڈریا کو تباہ کرنے کے لیے بھرتی کیا [37]۔ دیگر مطالعات سے پتہ چلتا ہے کہ HBV اور HBx پروٹین نے DRP1 کے اظہار کو فروغ دے کر mitochondrial fission کو فروغ دیا۔ HBV اور HBx پروٹین پارکن کی ثالثی مائٹوفگی کو متحرک کرنے کے ذریعے سیل کی بقا اور مسلسل وائرل انفیکشن کو بھی فروغ دیتے ہیں [37]۔ PB1-F2 انفلوئنزا وائرس کی روگجنکیت کے لیے ایک اہم وائرلیس عنصر ہے، جو کہ تھومیکسوویریڈے خاندان کا ایک لفافہ RNA وائرس ہے۔ PB1-F2 مائٹوکونڈریا کو نشانہ بناتا ہے اور اسے TOMM40 چینل کے ذریعے IMM تک پہنچایا جاتا ہے، جس سے مائٹوکونڈریل جھلی کی صلاحیت کا نقصان ہوتا ہے اور مائٹوکونڈریل فنکشن میں خلل پڑتا ہے [38–40]۔ اس کے برعکس، کم پیتھوجینک ذیلی قسم کا انفلوئنزا A PB1-F2، جس میں c-ٹرمینل ریجن کی کمی ہے، مائٹوکونڈریل ڈیسفکشن کا سبب نہیں بنتی ہے [41]۔ PB1-F2 مائٹوکونڈریا پر TUFM (Tu Translation elongation factor, mitochondrial) کے ساتھ تعامل کرتا ہے، mitophagy کی حوصلہ افزائی کرتا ہے، اور قسم I انٹرفیرون اظہار کو روکتا ہے [42]۔ تاہم، ایک حالیہ مطالعہ سے پتہ چلتا ہے کہ H1N1 انفیکشن مائٹوکونڈریل لمبائی کو فروغ دے سکتا ہے اور OPA1 اظہار کو بڑھا کر اور DRP1 اظہار کو کم کرکے میزبان سیل کے اینڈوپلاسمک ریٹیکولم – مائٹوکونڈریل رابطہ سائٹس کو تبدیل کر سکتا ہے، اس طرح مائٹوکونڈریل مورفولوجی کی حرکیات کو تبدیل کر سکتا ہے۔ اس کے علاوہ، Mito-C (ایک ناول پرو فیشن کمپاؤنڈ) کے ساتھ خلیات کے علاج نے مائٹوکونڈریل فنکشن [43] کے کچھ حصے کو بحال کرکے وائرل نقل کو نمایاں طور پر کم کیا۔ سیویئر ایکیوٹ ریسپائریٹری سنڈروم کورونا وائرس (SARS-CoV) ایک واحد پھنسے ہوئے مثبت پھنسے ہوئے RNA وائرس ہے جس کا تعلق جینس کورونا وائرس سے ہے۔ اس کا NSP2 PHB1 اور PHB2 کے ساتھ تعامل کرتا ہے، جو کئی سیلولر افعال میں ملوث ہے، اس طرح انٹرا سیلولر سگنلنگ کو متاثر کرتا ہے اور مائٹوکونڈریل بایوجنسیس [44,45] کو متاثر کرتا ہے۔ SARS-CoV وائرلیس عنصر ORF-9B بھی پروٹیزوم کے ذریعے DRP1 کو کم کرتا ہے، جس سے مائٹوکونڈریل فیوژن ہوتا ہے جو میزبان کے پیدائشی مدافعتی ردعمل سے بچ جاتا ہے [46]۔ شدید ایکیوٹ ریسپائریٹری سنڈروم کورونا وائرس 2 (SARS-CoV-2)، جو SARS-CoV کے طور پر ایک ہی خاندان کا رکن ہے، نے عالمی سماجی اور معاشی خلل پیدا کیا ہے۔ حالیہ مطالعات سے پتہ چلتا ہے کہ SARS-CoV-2 مدافعتی ردعمل اور سیل میٹابولزم کو جوڑ سکتا ہے تاکہ آٹوفیجی کو ریگولیٹ کر کے، ROS کے عمل کو بڑھا کر، اور مائٹوکونڈریل فنکشن کو کم کر کے سیل کی نقل کو فروغ دے سکے [47]۔ SARS-CoV-2 میں، ORF9b OMM پروٹین امپورٹ میکانزم [48] کے TOM70 ذیلی یونٹ کے ساتھ تعامل کرتا ہے، جس کا MAVS پر ممکنہ ریگولیٹری اثر ہوتا ہے۔ SARS-CoV-2 Nsp4، SARS-CoV میں CM کی تشکیل کے لیے ضروری ہے، ممکنہ طور پر مائٹوکونڈریل امپورٹ مشینری (TIM) کمپلیکس کے ساتھ تعامل کرتا ہے [48]۔ SARS-CoV-2 Nsp8 mitochondrial ribosomes [48] کے ساتھ بھی تعامل کرتا ہے۔ زیادہ سے زیادہ مطالعات سے پتہ چلتا ہے کہ وائرس مائٹوکونڈریل ڈائنامکس (شکل 1) کو جوڑ کر وائرل نقل کی ماحولیاتی سائٹس کو برقرار رکھتے ہیں۔ لہذا، وائرس اور مائٹوکونڈریل ڈائنامکس کا مطالعہ وائرل انفیکشن کے علاج کے لیے منشیات کے اہم اہداف بن سکتا ہے۔

تصویر 1. وائرل انفیکشن مائٹوکونڈریل ڈائنامکس میں خلل ڈالتا ہے۔ مختلف وائرس مائٹوکونڈریل فیوژن پروٹینز (MFNs, OPA1) یا فِشن پروٹینز (DRP1) کے ذریعے مائٹوکونڈریل ڈائنامکس کو متاثر کرتے ہیں اور خلیوں کی بقا اور وائرل استقامت کو بڑھانے کے لیے مائٹوفیجی کو نقصان پہنچا مائٹوکونڈریا کو صاف کرنے پر اکساتے ہیں۔
3. وائرل انفیکشن مائٹوکونڈریا کی وجہ سے سیل کی موت کو کنٹرول کرتا ہے۔

چینی جڑی بوٹی سیستانچ پلانٹ - اینٹیٹیمر
اپوپٹوس خلیوں کی خود مختاری اور پروگرام شدہ موت کا عمل ہے، جسے جینز کے ذریعے کنٹرول کیا جاتا ہے، تاکہ اندرونی ماحول کے استحکام کو برقرار رکھا جا سکے۔ فی الحال، سیل اپوپٹوسس کو تین راستوں میں تقسیم کیا جا سکتا ہے۔ مائٹوکونڈریا اندرونی اپوپٹوٹک راستے کے ذریعے سیل کی موت کو متاثر کرتا ہے۔ جب اپوپٹوس کی حوصلہ افزائی کی جاتی ہے، Bcl-2 فیملی پروٹین چینلز کا استعمال کرتے ہوئے مائٹوکونڈریل جھلی پروٹین کی ایکٹیویشن مائٹوکونڈریل بیرونی جھلی کی پارگمیتا کو متحرک کرتی ہے اور اپوپٹوس پروٹینز (جیسے Cyt c، Smac، وغیرہ) کو سائٹوپلازم میں جاری کرتی ہے۔ سائٹ سی اور اپوپٹوٹک پروٹیز ایکٹیوٹنگ فیکٹر 1 (اے پی اے ایف 1) آپس میں تعامل کرتے ہیں، اپوپٹوسمس بناتے ہیں اور پروکاسپیس کو چالو کرتے ہیں-9، جو کیسپیس-3 اور کیسپیس کو کریک کرتے ہیں-7، اس طرح سیل اپوپٹوسس [49] کو دلاتے ہیں۔ بہت سے وائرس سیل کی موت کو دلانے یا سیل کی موت کو روکنے کے ذریعے مسلسل انفیکشن کو برقرار رکھ کر وائرل پھیلاؤ کو فروغ دیتے ہیں۔ HCV مائٹوکونڈریل ڈائنامکس میں خلل ڈال کر سیل اپوپٹوس کو روکتا ہے۔ HCV انفیکشن DRP1Ser616 کے فاسفوریلیشن کو اکساتا ہے، جو mitochondrial fission اور mitophagy کو متحرک کرتا ہے، اس طرح سیل apoptosis کو روکتا ہے، جو بالآخر وائرل استقامت کو فروغ دیتا ہے [28]۔ CSFV انفیکشن HCV انفیکشن کی طرح ہے۔ CSFV اور HCV انفیکشن PINK1 اور Parkin کے راستے کو چالو کرنے کے ذریعے مائٹو فیگی کی موجودگی کو متحرک کرتا ہے تاکہ خراب مائٹوکونڈریا کو صاف کیا جا سکے اور پرو اپوپٹوٹک پروٹین کے اخراج کو روکا جا سکے، اس طرح سیل اپوپٹوسس کو روکتا ہے اور وائرل انفیکشن کو برقرار رکھتا ہے [28,31]۔ Drp1 سائلنسنگ مائٹوکونڈریل فِشن، مائٹوفگی، اور اپ ریگولیٹڈ اپوپٹوس سگنلز کو روکتا ہے جو HCV اور CSFV کے ذریعے حوصلہ افزائی کرتا ہے، جس سے وائرین سراو [28,31] کم ہوتا ہے۔ دلچسپ بات یہ ہے کہ ایچ سی وی وائرل پروٹین اپوپٹوس کو دلانے میں مختلف کردار ادا کرتے ہیں۔ مثال کے طور پر، NS4A پروٹین مائٹوکونڈریا کی انٹرا سیلولر تقسیم کو تبدیل کرتا ہے، جس سے مائٹوکونڈریل کو نقصان پہنچتا ہے اور سائٹ سی کو سائٹوپلازم میں چھوڑتا ہے، اس طرح Caspase-3-ثالثی اپوپٹوس کو چالو کرتا ہے [50]۔ E2 پروٹین، Huh-7 خلیوں میں منتقل ہوتا ہے، Bcl-2 کو نیچے ریگولیٹ کرتا ہے اور Bax کو اپ ریگولیٹ کرتا ہے، جو مائٹوکونڈریل پر منحصر کیسپیس پاتھ وے [51] کے ذریعے اپوپٹوس کو آمادہ کر سکتا ہے۔ بنیادی پروٹین کا 14-3-3ε پروٹین کے ساتھ تعامل اپوپٹوس کو چالو کرنے کے لیے بیکس کو جاری کرتا ہے [52]۔ NS4B مائٹوکونڈریل جھلی کی صلاحیت میں کمی کا سبب بنتا ہے، کیسپیس 9 کو چالو کرتا ہے، اور Cyt c کو جاری کرتا ہے، مائٹوکونڈریل موت کے راستے [53] کے ذریعے اپوپٹوسس کو اکساتا ہے۔ NS4A اور NS3-4ایک پروٹین Bax کو اپ ریگولیٹ کرتے ہیں اور مائٹوکونڈریا میں منتقل ہوتے ہیں، اینٹی اپوپٹوٹک پروٹین Bcl-xL کے اظہار کو نیچے ریگولیٹ کرتے ہیں اور کیسپیس کو چالو کرتے ہیں-9، اس طرح مائٹوکونڈریا میں ثالثی موت کو دلاتا ہے۔ بیکس اور کیسپیس جھرن ردعمل، جو بالآخر سیل کی موت کو اکساتا ہے [54]۔ وائرل پروٹین کے کام اور طریقہ کار اور وائرل پروٹین کی سرگرمی کو روکنے والے مادوں کے بارے میں مزید تحقیق دائمی ہیپاٹائٹس کے علاج اور منشیات کی نشوونما کے لیے نئے آئیڈیاز فراہم کر سکتی ہے۔ ایچ بی وی وائرس بھی اپوپٹوس کو متاثر کرتا ہے۔ HBx پروٹین مجموعی مائٹوکونڈریل ڈھانچے میں p53 کے ساتھ مضبوطی سے تعامل کر سکتا ہے، جس کی وجہ سے خلیے کی موت ہوتی ہے [55]۔ اسی طرح، DENV p53-منحصر مائٹوکونڈریا ثالثی اپوپٹوس [56] کو آمادہ کرتا ہے۔ Bax کے ساتھ پابند ہونے سے، HBx Bax اور 14-3-3epsilon کے درمیان تعامل میں مداخلت کرتا ہے، Bax کی mitochondria میں منتقلی کو بڑھاتا ہے، mitochondrial پارگمیتا ٹرانزیشن pores کے کھلنے کو منظم کرتا ہے اور Caspase-3 اور cytochrome C کو جاری کرتا ہے، اور پھر endogenous mitochondrial apoptosis [57,58] میں ثالثی کرنا۔ ایچ بی وی اپوپٹوس کو بھی روکتا ہے اور مائٹوکونڈریل ڈائنامکس کو تبدیل کرکے وائرل انفیکشن کو برقرار رکھتا ہے۔ HBx Mfn2 کے ہر جگہ ہونے کو آمادہ کر سکتا ہے، DRP1 کے اظہار کو فروغ دے سکتا ہے، مائٹوکونڈریل فِشن کا باعث بن سکتا ہے، اور PINK1-پارکن پاتھ وے کے ذریعے سیل اپوپٹوسس کو روک سکتا ہے اور سیل کی بقا اور وائرس کے مسلسل انفیکشن کو برقرار رکھتا ہے [37]۔ اس کے علاوہ، SARS-CoV سیل اپوپٹوس کو بھی آمادہ کر سکتا ہے۔ SARS-CoV 3a پروٹین کیسپیس کو چالو کر سکتا ہے-9 اور سائٹوکوم سی پروٹین کو مائٹوکونڈریا سے خارج کر سکتا ہے یا کیسپیس کو چالو کر سکتا ہے-8 خارجی سگنل (زبانوں) کے ذریعے اور مائٹوکونڈریل موت کے راستے کو ماڈیول کرنے کے لیے بولی کو چالو کر سکتا ہے [59]۔ SARS-CoV N پروٹین مائٹوکونڈریل جھلی کی صلاحیت میں کمی اور ROS اور cytochrome C کی ریلیز میں اضافے کو اکساتا ہے، جو apoptosis [59,60] میں ثالثی کرتا ہے۔ اس کے علاوہ، SARS-CoV M پروٹین mitochondrial cytochrome c پروٹین کی رہائی کو اکساتا ہے، جو سیل apoptosis [61] میں ثالثی کرتا ہے۔ اسی طرح، SARS-CoV-2 3ایک پروٹین apoptosis [48] کا باعث بن سکتا ہے۔ مزید یہ کہ وائرس سیل کی موت کو منظم کرکے نقل کو فروغ دے سکتے ہیں اور پھیل سکتے ہیں۔ مثال کے طور پر، Rotavirus، Reoviridae خاندان سے تعلق رکھنے والا ایک ڈبل پھنسے ہوئے RNA وائرس، apoptosis کو آمادہ کر سکتا ہے۔ حالیہ مطالعات سے پتہ چلتا ہے کہ NSP4 مائٹوکونڈریل جھلی پروٹین ایڈنائن نیوکلیوٹائڈ ٹرانسلوکیٹر اور وولٹیج پر منحصر اینون چینل (VDAC) کے ساتھ تعامل کے ذریعے مائٹوکونڈریل جھلی کی صلاحیت اور مائٹوکونڈریل پارگمیتا کو تبدیل کرتا ہے، سائٹوکوم سی کو جاری کرتا ہے، کیسپیس کو چالو کرتا ہے، اور میڈیا کو اپوٹوکونڈیریل میمبرین کو تبدیل کرتا ہے۔ سیل اپوپٹوسس [62]۔ اس کے علاوہ، روٹا وائرس انفیکشن بیکس کے ارتکاز کو ریگولیٹ کر سکتا ہے اور مائٹوکونڈریل پاتھ وے [63] کے ذریعے اپوپٹوس میں ثالثی کر سکتا ہے۔ دوسری طرف، روٹا وائرس انفیکشن کے ابتدائی مرحلے میں، NSP1 PI3K/Akt سگنلنگ پاتھ وے کو چالو کرکے یا p53 ریگولیشن کو روک کر اور سیل میں وائرس کی جلد نقل کو یقینی بنا کر سیل اپوپٹوسس کو روکتا ہے [64]۔ روٹا وائرس انفیکشن مائٹوکونڈریل ڈائنامکس کو ریگولیٹ کرکے اپوپٹوس میں بھی ثالثی کرتا ہے۔ روٹا وائرس انفیکشن کے آخری مرحلے میں، NSP4 CDK1 کے ذریعے Drp1 کے Ser616 فاسفوریلیشن کو اکساتا ہے اور DRP1 کو مائٹوکونڈریا میں بھرتی کرنے، مائٹوکونڈریل فریگمنٹیشن میں ثالثی، Cyt c کو جاری کرنے، اور کیسپیس کو چالو کرنے میں حصہ لیتا ہے-9 اور کیسپیس کو چالو کرنے میں۔ apoptosis دلانے اور وائرس کے پھیلاؤ کو آسان بنانے کے لیے [65]۔ اسی طرح، انفلوئنزا اے وائرلینس فیکٹر PB1-F2 IMM کو نشانہ بناتا ہے جو مائٹوکونڈریل dysfunction کا سبب بنتا ہے، اور endogenous mitochondrial pathway [38,66] کے ذریعے سیل کی موت کا باعث بنتا ہے۔ زیکا وائرس ایک واحد پھنسے ہوئے مثبت پھنسے ہوئے آر این اے وائرس ہے جس کا تعلق فلاوی وائرس جینس سے ہے، اور زیکا وائرس کا انفیکشن مائٹوکونڈریل ٹرانس میمبرین پوٹینشل کو بھی کم کر سکتا ہے، Mfn2 کے اظہار کو کم کر سکتا ہے، اور مائٹوکونڈریل فریگمنٹیشن کو فروغ دے سکتا ہے، جس سے سیل اپوپٹوسس ہوتا ہے۔ Mitochondrial division inhibitor 1 (Mdivi-1)، ایک چھوٹا مالیکیول جو mitochondria fission کو روکتا ہے، mitochondrial fission کو روکتا ہے اور Zika وائرس کے انفیکشن کے بعد mitochondrial حرکیات کو بہتر بناتا ہے، اس طرح سیل کی بقا میں اضافہ ہوتا ہے [67]۔ دلچسپ بات یہ ہے کہ سیلولر استثنیٰ سے بچنے کے لیے مختلف حکمت عملی وائرس میں تیار ہوئی ہے۔ مثال کے طور پر، وائرس انفیکشن سیل اپوپٹوس کو بہانے اور اس وجہ سے پھیلاؤ کی سہولت کے لیے آمادہ کر سکتا ہے۔ اس کے علاوہ، وائرس مائٹوفگی کے ذریعے سیل اپوپٹوسس کو روک سکتے ہیں، اس طرح ان کی نقل کو یقینی بنا سکتے ہیں۔ فی الحال، apoptosis اور autophagy کے درمیان طریقہ کار کو پوری طرح سے سمجھا نہیں گیا ہے، لیکن ہر عمل کا ضابطہ خلیات کو متوازن حالت میں رکھتا ہے [68,69]۔ متعدد مطالعات سے پتہ چلتا ہے کہ بہت سے وائرس اپوپٹوس کو روکنے کے لئے مائٹوفگی کو متحرک کرکے وائرل انفیکشن کو برقرار رکھ سکتے ہیں۔ HCV مائٹوفگی کے ذریعے فیشن مائٹوکونڈریا کو صاف کرتا ہے، اس طرح سیل اپوپٹوس کو روکتا ہے۔ ڈی آر پی 61 یا پارکن کو خاموش کرنا سائٹوکوم سی کے سراو کو بڑھا سکتا ہے، اپوپٹوس سگنلنگ میں نمایاں اضافہ اور کیسپیس 3 کی سرگرمی کو بڑھا سکتا ہے۔ یہ نتائج تجویز کرتے ہیں کہ ایچ سی وی مائٹوفگی [28] کے ذریعے اپوپٹوسس کو کم کرکے وائرل استقامت کو فروغ دیتا ہے۔ پورسائن ری پروڈکٹیو اینڈ ریسپائریٹری سنڈروم (PRRSV)، آرٹیرویریڈی فیملی کا ایک واحد مثبت اسٹرینڈ آر این اے وائرس، مائٹوکونڈریل ڈائنامکس میں خلل ڈال کر، مائٹوفیجی کو آمادہ کرکے، اور سیل اپوپٹوس [70] کو روک کر خود کی نقل کو فروغ دے سکتا ہے۔ HBV مائٹوکونڈریل فِشن اور مائٹوفیگی مالیکیولز کو اکساتا ہے، جو مائٹوکونڈریل فیشن اور مائٹوفگی میں ثالثی کرتے ہیں اور وائرس سے متاثرہ سیل اپوپٹوسس کو کم کرتے ہیں۔ مائٹوفگی کی پیداوار میں مداخلت اپوپٹوس سگنل کو بڑھاتا ہے اور وائرس کی نقل کو کم کرتا ہے [37]۔ اسی طرح، نیو کیسل ڈیزیز وائرس (NDV)، ایک واحد پھنسے ہوئے منفی RNA وائرس جو Paramyxoviridae خاندان سے تعلق رکھتا ہے، Porcine reproductive virus، اور CSFV مائٹوفگی کو آمادہ کرکے سیل اپوپٹوسس کو روک سکتا ہے، اس طرح وائرس کے انفیکشن کو فروغ دیتا ہے [31,71]۔ وائرل انفیکشن کے تناظر میں، apoptosis mitophagy کو کیسے منظم کرتا ہے اور apoptosis اور mitophagy کے درمیان باہمی ضابطے کے مالیکیولر میکانزم کو مزید مطالعہ کی ضرورت ہے۔ آخر میں، مائٹوکونڈریل پاتھ وے کے ذریعے اپوپٹوسس کو اکسانے والے وائرس خود نقل کی جگہ کو برقرار رکھتے ہیں (شکل 2)۔ لہذا، وائرس سے متاثرہ سیل اپوپٹوسس کے مخصوص طریقہ کار پر مزید تحقیق مختلف وائرسوں کے لیے نئی اینٹی وائرل ادویات کی سہولت فراہم کرے گی۔
4. وائرل انفیکشن مائٹوکونڈریا سے متاثرہ پیدائشی قوت مدافعت کو منظم کرتا ہے۔

مردوں کے لئے cistanche فوائد - مدافعتی نظام کو مضبوط
Cistanche Enhance Immunity مصنوعات دیکھنے کے لیے یہاں کلک کریں۔
【مزید پوچھیں】 ای میل:cindy.xue@wecistanche.com / واٹس ایپ: 0086 18599088692 / وی چیٹ: 18599088692
جب کوئی وائرس خلیات کو متاثر کرتا ہے، تو میزبان پیتھوجین ریکگنیشن ریسیپٹرز (PRRs) جیسے TLRs، RLRs اور NLRs کے ذریعے وائرس کو پہچاننے کے لیے پیدائشی مدافعتی نظام کو متحرک کرتا ہے۔ یہاں، ہم وائرل انفیکشن پر توجہ مرکوز کرتے ہیں جو مائٹوکونڈریا ثالثی آر ایل آر سگنلنگ پاتھ وے کو ریگولیٹ کرتے ہیں۔ بہت سے وائرل پیتھوجین سے وابستہ مالیکیولر پیٹرن (PAMPs) کو retinoic acid-inducible gene I (RIG-I) اور میلانوما تفریق سے وابستہ جین 5 (MDA5) سے پہچانا جاتا ہے۔ RIG-1 اور MDA5 تعمیری تبدیلیوں سے گزرتے ہیں جس کے نتیجے میں CARD ڈومین ایک ہم جنس اولیگومر کی شکل میں ظاہر ہوتا ہے۔ RIG-1 اور MDA5 N-ٹرمینل کارڈ ڈومین اور MAVS کے N-ٹرمینل کارڈ ڈومین کے ذریعے ایک دوسرے کو پہچانتے اور باندھتے ہیں، MAVS prion نما پولیمر بناتے ہیں اور NF-κB اور IRF3/ جیسے نیچے کی طرف سگنلنگ کے راستوں کو چالو کرتے ہیں۔ 7، اس طرح فطری اینٹی وائرل ردعمل میں شامل سوزش والی سائٹوکائنز اور انٹرفیرون کے اظہار کو اکساتا ہے۔ MAVS RLR پاتھ وے کے اہم اڈاپٹر پروٹین کے طور پر OMM میں واقع ہے۔ MAVS کے افعال اس کے مائٹوکونڈریل لوکلائزیشن پر منحصر ہیں، اس بات کی تصدیق کرتے ہیں کہ مائٹوکونڈریا پیدائشی مدافعتی سگنلنگ راستے میں اہم کردار ادا کرتا ہے۔

تصویر 2۔ وائرل انفیکشن مائٹوکونڈریا کی وجہ سے سیل کی موت کو کنٹرول کرتا ہے۔ مختلف وائرس B-cell lymphoma 2 (Bcl-2) فیملی پروٹین میں ثالثی کرتے ہیں، Cyt c کو جاری کرتے ہیں، پروکاسپیس کو چالو کرتے ہیں-9، اور apoptosomes بناتے ہیں، اس طرح سیل apoptosis کو جنم دیتے ہیں۔
زیادہ سے زیادہ مطالعات سے پتہ چلتا ہے کہ وائرسوں نے اپنے ارتقاء کے دوران مائٹوکونڈریا میں RLR سگنلنگ پاتھ وے کو میزبان کے مدافعتی نظام سے بچنے کے لیے حکمت عملیوں کا ایک سلسلہ تیار کیا (شکل 3)۔ SARS-CoV 3b پروٹین MAVS سرگرمی کو روک کر قسم I IFN کی پیداوار کو روکتا ہے [72]۔ اس کے علاوہ، SARS-CoV-2 کا Nsp13 پروٹین اور 9C پروٹین MAVS سگنل کی منتقلی کے ضابطے میں شامل ہو سکتے ہیں، اس طرح پیدائشی مدافعتی ردعمل میں ثالثی کرتے ہیں [48]۔ ایک حالیہ تحقیق سے پتہ چلتا ہے کہ SARS-CoV{10}} انسانی بڑی آنت کے کینسر کے خلیات Caco-2 میں انفیکشن کے نتیجے میں MAVS [73] کے اظہار میں کمی واقع ہوئی۔ HCV میزبان استثنیٰ سے بچ سکتا ہے، دائمی انفیکشن کا باعث بنتا ہے۔ NS3/4A کو مائٹوکونڈریا میں مقامی کیا جا سکتا ہے اور MAVS کے ساتھ ملایا جا سکتا ہے۔ NS3/4A MAVS کو Cys- 508 میں توڑ دیتا ہے، جس کی وجہ سے MAVS کا N-ٹرمینل ٹکڑا مائٹوکونڈریا سے الگ ہو جاتا ہے اور ایک غیر فعال ٹکڑا بن جاتا ہے، جو IFN [74,75] کی پیداوار کو روکتا ہے۔ اسی طرح، Bat Hepatovirus اور Seneca Valley وائرس RNA وائرس ہیں، دونوں کا تعلق Picornaviridae خاندان سے ہے، جو MAVs پروٹین کے ساتھ تعامل کرکے پیدائشی مدافعتی سگنل کی منتقلی میں بھی مداخلت کر سکتے ہیں، اس طرح وائرل انفیکشن [76,77] کو برقرار رکھتے ہیں۔ Bat Hepatovirus 3ABC پروٹیز انسانی MAVS کے ساتھ تعامل کرتے ہیں اور Glu463/Gly464 پر MAVS کو IRF3 اور NF-κB کے ایکٹیویشن کو روکتے ہیں، اس طرح انسانی خلیوں میں قسم I انٹرفیرون کی پیداوار کو روکتے ہیں [76]۔ سینیکا ویلی وائرس 3C پروٹیز Q148 پر MAVS کو صاف کرنے کے لئے اس کی پروٹیز سرگرمی پر منحصر ہے، قسم I انٹرفیرون [77] کو روکتا ہے۔ اس کے علاوہ، وائرس پروٹیزوم پاتھ وے کے ذریعے MAVS کو بھی نیچا کر سکتا ہے اور RLR سگنلنگ پاتھ وے کو روک سکتا ہے۔ مثال کے طور پر، HBV HBx پروٹین MAVS کے ساتھ تعامل کر سکتا ہے، MAVS کے ہر جگہ ہونے اور انحطاط کو فروغ دے سکتا ہے، اور RIG-I-MDA5 کے راستے کو روک سکتا ہے، جو مل کر IFN- [78] کی پیداوار کو کم کرتا ہے۔ NDV V پروٹین E3 ubiquitin ligase RNF5 کو بھرتی کرتا ہے تاکہ IFN کی پیداوار [79] کو روکنے کے لیے پروٹاسومل راستے کے ذریعے MAVS انحطاط میں ثالثی کرے۔ روٹا وائرس VP3 پروٹین مائٹوکونڈریا کو نشانہ بناتا ہے اور MAVS کے پرولین سے بھرپور خطے میں SPLTSS شکل کے فاسفوریلیشن میں ثالثی کرتا ہے، جس کی وجہ سے MAVS پروٹیزوم پاتھ وے کے ذریعے انحطاط پذیر ہوتا ہے، آنتوں کے اپکلا خلیوں کے روٹا وائرس انفیکشن کے دوران IFN- کی پیداوار کو روکتا ہے [80]۔ وائرس MAVS کے RIG-1 اور MDA5 کے پابند ہونے کو روک کر RLR سگنلنگ پاتھ وے کو بھی روکتے ہیں۔ 14-3-3-بائنڈنگ موٹف کے پابند ہونے سے، زیکا وائرس NS3 RIG-1 اور MDA5 کو مائٹوکونڈریا میں منتقل ہونے سے روکتا ہے، اس طرح RLR سگنلنگ پاتھ وے [81] کے ذریعے ثالثی انٹرفیرون کی پیداوار کو روکتا ہے۔ DENV NS4A MAVS کے N-terminal CARD-like (CL) ڈومین اور C-terminal transmembrane (TM) ڈومین سے منسلک ہے، جو MAVS کو RIG-I کے پابند ہونے سے روکتا ہے اور انٹرفیرون کی پیداوار کو روکتا ہے [82]۔ وائرس مائیکرو آر این اے میں ہیرا پھیری کرکے، RLR سگنلنگ کے راستوں کو روکنے کے لیے پوسٹ ٹرانسکرپشن ریگولیشن کے ذریعے میزبان مدافعتی نظام کی ایک رینج کو ریگولیٹ کرکے میزبان فطری قوت مدافعت سے بھی بچ سکتے ہیں۔ Vesicular Stomatitis Virus (VSV)، خاندان Rhabviridae کا ایک واحد پھنسے ہوئے منفی RNA (ssRNA) وائرس، انفیکشن IRF3 کے ذریعے miR-576-3پی کو اکساتا ہے اور MAVS اور TRAF3 mRNAs کو ریگولیٹ کرتا ہے تاکہ ٹائپ I اظہار انٹرفیرون کو کم کیا جا سکے اور ضرورت سے زیادہ سوزش سے بچا جا سکے۔ 83]۔ Rhabdovirus بہت سے croaker macrophages کو متاثر کرتا ہے، miR-3570 اظہار کو متاثر کرتا ہے اور MAVS اظہار کو نشانہ بناتا اور دباتا ہے، اس طرح وائرس کو فروغ دیتا ہے [84]۔ مطالعات سے پتہ چلتا ہے کہ وائرل انفیکشن کی وجہ سے پیدا ہونے والے miR-302b اور miR-372 اسپارٹیٹ گلوٹامیٹ ٹرانسپورٹر SLC25A12 کے ذریعے سیل کے فنکشن اور مائٹوکونڈریل میٹابولزم میں ہیرا پھیری کر سکتے ہیں، اس طرح اینٹی وائرل وائرسز [85] کے خلاف MAVS کی ثالثی کی پیدائشی قوت مدافعت کو خراب کر سکتے ہیں۔ دلچسپ بات یہ ہے کہ خلیوں میں miR-302b اور miR-372 کی نقل کا تعارف NADH کی سطح کو کم کر سکتا ہے، جس کے نتیجے میں NAD/NADH تناسب میں 50% تک اضافہ ہوتا ہے، مائٹوکونڈریل آکسیجن کی کھپت میں کمی واقع ہوتی ہے۔ ، اور بالآخر سیلولر میٹابولک راستوں میں سائٹرک ایسڈ سائیکل سے شوگر کے عمل انہضام میں تبدیلی، جبکہ لییکٹیٹ کے مواد میں اضافہ ہوتا ہے [85]۔ تازہ ترین تحقیق سے پتہ چلتا ہے کہ ہیپاٹائٹس بی وائرس کا انفیکشن براہ راست MAVS سے لییکٹیٹ ڈیہائیڈروجنیز پر منحصر لیکٹک ایسڈ کے ذریعے جڑتا ہے تاکہ MAVS کو مائٹوکونڈریل ایگریگیشن اور لوکلائزیشن سے روکا جا سکے، اس طرح RLR سگنلنگ پاتھ وے [86] کو روکا جاتا ہے۔ چونکہ لییکٹک ایسڈ بچھڑے کی ثالثی کے پیدائشی مدافعتی ردعمل [87] میں منفی ریگولیٹری کردار ادا کرتا ہے، یہ دو miRNAs لیکٹک ایسڈ ریگولیشن کے ذریعے پیدائشی قوت مدافعت کو متاثر کر سکتے ہیں۔
5. وائرل انفیکشن مائٹوکونڈریل میٹابولزم کو منظم کرتا ہے۔
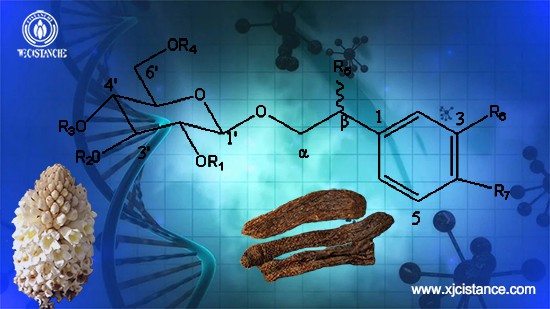
Phenylethanol glycoside Cistanche deserticola کا اہم فعال جزو ہے۔
مائٹوکونڈریا خلیات کے توانائی کے تحول کے مراکز ہیں۔ وہ کاربوہائیڈریٹس، امینو ایسڈز اور فیٹی ایسڈز کے میکرومولیکولر میٹابولزم کو منظم کرکے اے ٹی پی تیار کرتے ہیں۔ سیل کا بنیادی توانائی کا ذریعہ اے ٹی پی مالیکیول کے ذریعہ اڈینوسین ڈائی فاسفیٹ (ADP) مالیکیول میں ڈیفاسفوریلیٹ ہوتا ہے۔ اس عمل کو جاری رکھنے کے لیے، خلیوں کو کچھ میکرومولیکولر میٹابولائٹس کو راستے جیسے گلیکولائسز، ٹرائکاربو آکسیلک ایسڈ سائیکل، اور آکسیڈیٹیو فاسفوریلیشن کے ذریعے توڑنے کی ضرورت ہے۔ گلوکوز خلیوں کے لئے توانائی کا بنیادی ذریعہ ہے۔ سائٹوپلازم میں، اے ٹی پی کے دو مالیکیول گلوکوز کے ایک مالیکیول سے گلائکولائسز کے ذریعے پیدا ہوتے ہیں، جس سے دو پائروویٹ مالیکیول پیدا ہوتے ہیں۔ ATP کی پیداوار کو بہتر بنانے کے لیے، خلیات آکسیڈیٹیو فاسفوریلیشن (OXPHOS) سے گزرتے ہیں، جو ٹرائی کاربو آکسیلک ایسڈ سائیکل کے ساتھ مائٹوکونڈریل پائروویٹ کیریئر (MPC) کے ذریعے پائروویٹ کو مائٹوکونڈریل میٹرکس میں آکسائڈائز کرتا ہے۔ آخر میں، مائٹوکونڈریل الیکٹران ٹرانسپورٹ چین کے ذریعے ایک گلوکوز مالیکیول کا مکمل آکسیکرن 36 اے ٹی پی مالیکیولز پیدا کرتا ہے۔ اگرچہ آکسیڈیٹیو فاسفوریلیشن اعلی توانائی کی کارکردگی پیدا کرتا ہے، لیکن یہ ایک سست عمل ہے اور تیزی سے تقسیم ہونے والے خلیوں کی توانائی کی ضروریات کو پورا نہیں کر سکتا، جیسے فعال مدافعتی خلیات یا کینسر کے خلیات۔ لہذا، ان خلیوں کو اپنی سرگرمی کو برقرار رکھنے کے لیے تیزی سے توانائی پیدا کرنے کے لیے ایروبک گلائکولائسز (جسے واربرگ اثر بھی کہا جاتا ہے) شروع کرنے کی ضرورت ہے۔ مزید برآں، فاقہ کشی اور ایمرجنسی کے دوران، لیپیز لپڈز کو مفت فیٹی ایسڈز میں تبدیل کرتا ہے، جو فیٹی ایسڈ آکسیڈیشن کے لیے مائٹوکونڈریا میں داخل ہوتے ہیں، اس طرح سیلولر انرجی میٹابولزم کا توازن برقرار رہتا ہے۔

تصویر 3۔ وائرل انفیکشن مائٹوکونڈریا سے پیدا ہونے والی پیدائشی قوت مدافعت کو منظم کرتا ہے۔ وائرس کے سیل پر حملہ کرنے کے بعد، RLRs وائرل RNA کو پہچانتے ہیں اور اینٹی وائرل سگنل پاتھ وے کو چالو کرنے کے لیے مائٹوکونڈریل اینٹی وائرل سگنل (MAVS) کے ساتھ تعامل کرتے ہیں۔ مختلف وائرس RLR سگنلنگ پاتھ وے کو مسدود کرکے میزبان کی پیدائشی قوت مدافعت سے بچ جاتے ہیں۔
بہت سے وائرس انٹرا سیلولر بقا کو بڑھانے کے لیے میزبان سیل میٹابولزم کو فعال طور پر نئی شکل دے سکتے ہیں۔ ایچ سی وی انفیکشن سیل میٹابولزم میں تبدیلیوں کا سبب بنتا ہے، جو گلائکولائسز کے دوران کاربوہائیڈریٹ کے اخراج کو بڑھاتا ہے اور ایروبک آکسیڈیٹیو فاسفوریلیشن اور سائٹرک ایسڈ سائیکل کی سرگرمیوں کو کم کرتا ہے، جو کہ خلیے کو تیزی سے واربرگ ایفیکٹ کی طرف لے جا سکتا ہے، انفیکشن کے چند دنوں یا ہفتوں کے اندر۔ ایک سیل [88–90]۔ ایک حالیہ تحقیق میں، مائٹوکونڈریل ریسپائریٹری چین کمپلیکس کے کچھ اہم اجزاء HCV انفیکشن کے چھ دن بعد نیچے ریگولیٹ پائے گئے، بشمول MT-ND1، MT-ND3، MT-ND4، MT-ND4L، اور MT-CO2 [91۔ ] اس کے علاوہ، MTND، COX، اور F0/F1ATP سنتھیس کا ڈاؤن ریگولیشن HCV سے متاثرہ CD8+T سیل سائیکل [92,93] میں پایا گیا۔ یہ دکھایا گیا ہے کہ HCV منظم طریقے سے mitochondrial respiratory chain complex [94] کے اظہار کو تبدیل کرکے آکسیڈیٹیو فاسفوریلیشن کی سرگرمی کو محدود کرتا ہے۔ HIF-1 اور proto-oncogene c-myc کا HCV سے متاثرہ خلیوں میں نمایاں طور پر اظہار کیا جاتا ہے، جس سے گلوکوکنیز (GK)، فاسفوگلوکوز-1 (PFK{{27}) سمیت کئی گلائکولٹک کلیدی خامروں کا اظہار ہوتا ہے۔ })، اور پائروویٹ کناز (PK) [95-97]۔ اس کے علاوہ، HCV انفیکشن Hexokinase 2 اظہار کو اپ گریجولیشن پر اکساتا ہے اور HCV پروٹین NS5a [98] کے ساتھ تعامل کے ذریعے Hexokinase سرگرمی کو بڑھاتا ہے۔ DENV انفیکشن گلوکوز ٹرانسپورٹر 1 اور hexokinase 2 [99] کی اپ گریجشن کو بھی آمادہ کرتا ہے۔ گلائکولیٹک پاتھ وے کی روک تھام نے DENV کی RNA ترکیب اور متعدی وائرس کی پیداوار کو نمایاں طور پر کم کر دیا، جس سے یہ ظاہر ہوتا ہے کہ DENV اپنی نقل کو برقرار رکھنے کے لیے سیلولر گلائکولائسز کو دوبارہ تشکیل دے سکتا ہے [99]۔ دلچسپ بات یہ ہے کہ DENV پروٹین کے میزبان میٹابولزم پر مختلف اثرات ہوتے ہیں۔ DENV NS1 پروٹین GAPDH کے ساتھ بات چیت کرتا ہے تاکہ GADPH [100] کی گلیکولیٹک سرگرمی کو بڑھا سکے۔ تاہم، GAPDH کے ساتھ DENV NS3 پروٹین کے تعامل کے نتیجے میں GAPDH glycolysis کی سرگرمی کم ہوئی [101]۔ HCV اور DENV انفیکشن سیل میٹابولزم کو نئی شکل دے سکتے ہیں، مائٹوکونڈریل فیٹی ایسڈ آکسیڈیشن کو بڑھا سکتے ہیں، اور توانائی فراہم کر سکتے ہیں [102–104]۔ دریں اثنا، مائٹوکونڈریا میں فیٹی ایسڈ کی نقل و حمل کی روک تھام اور آکسیڈیشن کا ضابطہ وائرل نقل کو متاثر کر سکتا ہے [103]۔ زیکا وائرس میزبان وسائل کو استعمال کر سکتا ہے اور مختلف خلیوں میں سیل میٹابولزم کو دوبارہ پروگرام کر سکتا ہے تاکہ مختلف میٹابولک راستوں میں خلیے کی حالت کو منظم کیا جا سکے، اس طرح اس کی خود ساختہ نقل [105-108] میں آسانی ہوتی ہے۔ ایچ آئی وی CD4+ T خلیوں میں نقل کرتا ہے اور آکسیڈیٹیو فاسفوریلیشن سے ایروبک گلائکولائسز [109] تک میٹابولک ری پروگرامنگ کا باعث بنتا ہے۔ ایچ آئی وی انفیکشن گلوکوز ٹرانسپورٹر کے بڑھنے، زیادہ گلوکوز کے اخراج، اور گلائکولیٹک انزائمز لییکٹیٹ ڈیہائیڈروجنیز اے (LDHA) ہیکسوکینیز-1 کے اپ ریگولیشن کو اکساتا ہے، اس طرح ایروبک گلائکولائسز کو چالو کرتا ہے، جو اس کے لیے سازگار ہے۔ ایچ آئی وی ریورس ٹرانسکرپشن، انضمام، اور ویرون کی پیداوار [110-113]. ایروبک گلائکولائسز کو بڑھانے کے علاوہ، HIV سے متاثرہ CD4+ T خلیات گلوٹامین میٹابولزم کا سبب بن سکتے ہیں اور پیداواری HIV انفیکشن [114,115] کے دوران گلوٹامین کا دوبارہ استعمال کر سکتے ہیں۔ بنیادی توانائی کے ذرائع کے طور پر گلوکوز اور گلوٹامین کے علاوہ، ایچ آئی وی فیٹی ایسڈ آکسیڈیشن کو توانائی کے ذریعہ کے طور پر CD4+ T خلیات کو متاثر کرنے کے لیے استعمال کرتا ہے [115]۔ ایک حالیہ مطالعہ سے پتہ چلتا ہے کہ ایچ آئی وی انفیکشن ایروبک گلائکولائسز کو اکساتا ہے، جو انفیکشن کو برقرار رکھنے کے لیے ذرات میں پیک کیے گئے عوامل کو کنٹرول کرکے وائرس کے معیار کو کنٹرول کرنے میں مدد کرتا ہے [116]۔ اگرچہ مائٹوکونڈریل میٹابولزم کا وائرل انفیکشن سے گہرا تعلق ہے، لیکن وہ طریقہ کار جس کے ذریعے وائرس مائٹوکونڈریل میٹابولزم کو نشانہ بناتے ہیں اور وائرس سیل میٹابولزم سے پیدا ہونے والی توانائی کو کس طرح استعمال کرتے ہیں یہ ابھی تک واضح نہیں ہے۔
6. اختتامی ریمارکس
پچھلی چند دہائیوں کے دوران، مائٹوکونڈریا کو وائرل انفیکشن اور میزبان فطری قوت مدافعت میں اہم کردار ادا کرتے ہوئے دکھایا گیا ہے۔ تاہم، میزبان – وائرس کے تعامل میں مائٹوکونڈریا کے کردار کا مزید مطالعہ کرنے کی ضرورت ہے۔ وائرل انفیکشن مائٹوکونڈریل فنکشن میں ہیرا پھیری کرکے اپنے لیے ایک قابل عمل ماحولیاتی مقام بنا سکتے ہیں۔ وائرس مائٹوکونڈریا کی حوصلہ افزائی سیل کی موت اور مائٹوکونڈریا کی ثالثی کے پیدائشی مدافعتی نظام کو مائٹوکونڈریل حرکیات کو ریگولیٹ کرکے اس کی نقل اور منتقلی کی سہولت فراہم کرتا ہے۔ حالیہ برسوں میں، سیل میٹابولزم کے ریگولیٹری مرکز کے طور پر مائٹوکونڈریا کے کردار نے زیادہ توجہ مبذول کرائی ہے۔ وائرس سیل میٹابولزم میں ہیرا پھیری کر سکتے ہیں، میٹابولک راستوں کو دوبارہ پروگرام کر سکتے ہیں، اور خلیوں میں وائرل طاقوں کو برقرار رکھنے کے لیے میٹابولائٹس کو دوبارہ استعمال کر سکتے ہیں۔ تاہم، مائٹوکونڈریا اور ان کے میٹابولزم پر تحقیق ابھی ابتدائی مراحل میں ہے۔ ان میکانزم کا پتہ لگانا جن کے ذریعے وائرس انفیکشن کو برقرار رکھنے کے لیے مائٹوکونڈریا ثالثی سیل میٹابولزم کا استعمال کرتے ہیں مستقبل کی تحقیق کے لیے ایک دلچسپ علاقہ ہے۔
حوالہ جات
1. کریاما، Y.؛ Nochi, H. انٹرا- اور انٹر سیلولر کوالٹی کنٹرول میکانزم آف مائٹوکونڈریا۔ سیلز 2017، 7، 1۔ [کراس ریف] [پب میڈ]
2. ہیلز، کلوگرام؛ فلر، ایم ٹی ڈویلپمنٹلی ریگولیٹڈ مائٹوکونڈریل فیوژن ایک محفوظ، ناول، پیشن گوئی شدہ GTPase کے ذریعے ثالثی کی گئی۔ سیل 1997، 90، 121–129۔ [کراس ریف]
3. چن، ایچ. Detmer, SA; Ewald, AJ; گرفن، ای ای؛ فریزر، SE؛ Chan, DC Mitofusins Mfn1 اور Mfn2 ہم آہنگی سے مائٹوکونڈریل فیوژن کو منظم کرتے ہیں اور جنین کی نشوونما کے لیے ضروری ہیں۔ جے سیل بائیول۔ 2003، 160، 189–200۔ [کراس ریف]
4. چن، ایچ. چومین، اے. چان، ڈی سی فیوژن میں خلل کے نتیجے میں مائٹوکونڈریل ہیٹروجنیٹی اور dysfunction ہوتا ہے۔ J. Biol کیم 2005، 280، 26185–26192۔ [کراس ریف]
5. Cipolat, S.; مارٹنز ڈی بریٹو، او۔ دال زیلیو، بی۔ Scorrano، L. OPA1 کو مائٹوکونڈریل فیوژن کو فروغ دینے کے لیے mitofusin 1 کی ضرورت ہے۔ پروک ناٹل اکاد۔ سائنس USA 2004، 101، 15927–15932۔ [کراس ریف] [پب میڈ]
6. کوشیبا، ٹی. Detmer, SA; قیصر، جے ٹی؛ چن، ایچ. McCaffery, JM; چان، ڈی سی ساختی بنیاد مائٹوکونڈریل ٹیتھرنگ بذریعہ مائٹوفوسین کمپلیکس۔ سائنس 2004، 305، 858–862۔ [کراس ریف]
7. Cao, YL; مینگ، ایس. چن، وائی؛ فینگ، جے ایکس؛ گو، ڈی ڈی؛ یو، بی؛ لی، وائی جے؛ یانگ، جے وائی؛ لیاو، ایس. چان، ڈی سی؛ ET رحمہ اللہ تعالی. Mfn1 ڈھانچے مائٹوکونڈریل فیوژن کے لئے نیوکلیوٹائڈ سے متحرک ڈائمرائزیشن کو ظاہر کرتے ہیں۔ فطرت 2017، 542، 372–376۔ [کراس ریف]
8. اوٹیرا، ایچ. میہارا، K. مالیکیولر میکانزم اور مائٹوکونڈریل ڈائنامکس کے فزیولوجک افعال۔ جے بائیو کیم۔ 2011، 149، 241–251۔ [کراس ریف]
9. روزو، ایم؛ لیگروس، ایف۔ Chateau، D.؛ Lombès، A. میمبرین ٹوپولوجی اور مائٹوکونڈریل ٹارگٹنگ آف مائٹوفوسینز، ٹرانس میمبرن کے ہر جگہ موجود ممالیہ ہومولوگز۔ جے سیل سائنس GTPase Fzo۔ 2002، 115، 1663–1674۔
10. آنند، آر. وائی، ٹی. بیکر، ایم جے؛ Kladt, N.; Schauss, AC; Rugarli, E.; لینگر، T. i-AAA پروٹیز YME1L اور OMA1 OPA1 کو مائٹوکونڈریل فیوژن اور فیوژن کو متوازن کرنے کے لیے کلیو کرتا ہے۔ جے سیل بائیول۔ 2014، 204، 919-929۔ [کراس ریف] [پب میڈ]
11۔ ٹونڈرا، ڈی۔ گرینڈیمینج، ایس. جورڈین، اے. کاربوسکی، ایم. Mattenberger, Y.; ہرزگ، ایس. دا کروز، ایس. کلرک، پی. Raschke، I.؛ مرک ورتھ، سی۔ ET رحمہ اللہ تعالی. SLP-2 تناؤ سے متاثر مائٹوکونڈریل ہائپر فیوژن کے لیے درکار ہے۔ ای ایم بی او جے 2009، 28، 1589–1600۔ [کراس ریف] [پب میڈ]
12. Ingerman, E.; پرکنز، ای ایم؛ مارینو، ایم؛ میئرز، جے اے؛ McCaffery, JM; ہنشا، جے ای؛ نوناری، J. Dnm1 سرپل بناتا ہے جو ساختی طور پر فٹ مائٹوکونڈریا کے مطابق ہوتا ہے۔ جے سیل بائیول۔ 2005، 170، 1021–1027۔ [کراس ریف]
13. جی، ڈبلیو کے؛ ہیچ، AL؛ میرل، RA؛ سٹریک، ایس. ہِگز، ایچ این ایکٹین فلیمینٹس ڈائنامین GTPase Drp1 کی oligomeric maturation کو mitochondrial fission sites پر نشانہ بناتے ہیں۔ Elife 2015, 4, e11553. [کراس ریف] [پب میڈ]
14. تگوچی، این. اشیہارا، این. جوفوکو، اے. اوکا، ٹی. میہارا، K. ڈائنامین سے متعلق GTPase Drp1 کا مائٹوٹک فاسفوریلیشن مائٹوکونڈریل فیزیشن میں حصہ لیتا ہے۔ J. Biol کیم 2007، 282، 11521–11529۔ [کراس ریف] [پب میڈ]
15. سیٹو، ٹی. ناہ، جے. اوکا، ایس آئی؛ مکئی، آر. Monden, Y.; Maejima, Y.; Ikeda, Y.; Sciarretta, S.; لیو، ٹی. لی، ایچ. ET رحمہ اللہ تعالی. Rab9 کی طرف سے ثالثی کا متبادل مائٹوفگی راستہ دل کو اسکیمیا سے بچاتا ہے۔ جے کلین تفتیش کریں۔ 2019، 129، 802–819۔ [کراس ریف]
16. چانگ، سی آر؛ بلیک اسٹون، C. Drp1 کا سائیکلک AMP پر منحصر پروٹین کناز فاسفوریلیشن اس کی GTPase سرگرمی اور mitochondrial مورفولوجی کو منظم کرتا ہے۔ J. Biol کیم 2007، 282، 21583–21587۔ [کراس ریف] [پب میڈ]
17. ریکٹر، وی. سنگھ، اے پی؛ Kvansakul، M.؛ ریان، ایم ٹی؛ Osellame، LD پاور ہاؤس کو تقسیم کرنا: mitochondrial fission کے طریقہ کار میں ساختی بصیرت۔ سیل Mol. لائف سائنس. 2015، 72، 3695–3707۔ [کراس ریف]
18. یون، وائی. کروگر، ای ڈبلیو؛ اوسوالڈ، بی جے؛ میک نیوین، ایم اے مائٹوکونڈریل پروٹین ایچ ایف آئی ایس 1 ممالیہ کے خلیوں میں مائٹوکونڈریل فیشن کو ڈائنامین نما پروٹین DLP1 کے ساتھ تعامل کے ذریعے منظم کرتا ہے۔ مول سیل بائیول۔ 2003، 23، 5409–5420۔ [کراس ریف]
19. اوٹیرا، ایچ. وانگ، سی. کلیلینڈ، ایم ایم؛ سیٹوگوچی، K.؛ یوکوٹا، ایس. یول، آر جے؛ Mihara, K. Mff ممالیہ خلیوں میں mitochondrial fission کے دوران Drp1 کی mitochondrial بھرتی کے لیے ایک ضروری عنصر ہے۔ جے سیل بائیول۔ 2010، 191، 1141–1158۔ [کراس ریف]
20. یو، آر. جن، ایس بی؛ لینڈہل، یو۔ نیسٹر، ایم؛ Zhao, J. Human Fis1 فیوژن مشینری کی روک تھام کے ذریعے mitochondrial حرکیات کو منظم کرتا ہے۔ EMBO J. 2019, 38, e99748. [کراس ریف]
21. پامر، CS؛ Osellame, LD; لین، ڈی. Koutsopoulos, OS; Frazier, AE; ریان، MT MiD49 اور MiD51، مائٹوکونڈریل فِشن مشینری کے نئے اجزاء۔ EMBO Rep. 2011, 12, 565–573. [کراس ریف]
22. زاؤ، جے؛ لیو، ٹی. جن، ایس. وانگ، ایکس؛ کیو، ایم؛ Uhlén، P.؛ ٹومیلن، این. شوپلیاکوف، او۔ لینڈہل، یو۔ Nistér, M. Human MIEF1 Drp1 کو مائٹوکونڈریل بیرونی جھلیوں میں بھرتی کرتا ہے اور فیوژن کے بجائے مائٹوکونڈریل فیوژن کو فروغ دیتا ہے۔ EMBO J. 2011, 30, 2762–2778. [کراس ریف]
23. باربارو، جی؛ ڈی لورینزو، جی؛ Asti, A.; ربرسانی، ایم. بیلونی، جی؛ گریگوریو، بی؛ فلیس، جی؛ باربرینی، جی۔ دائمی ہیپاٹائٹس سی کے مریضوں میں ہیپاٹو سیلولر مائٹوکونڈریل تبدیلیاں: الٹراسٹرکچرل اور بائیو کیمیکل نتائج۔ ایم۔ J. Gastroenterol. 1999، 94، 2198–2205۔ [کراس ریف]
24. Schwer, B.; رین، ایس. Pietschmann, T.; کارٹن بیک، جے؛ Kaehlcke, K.; Bartenschlager, R.; ین، ٹی ایس؛ اوٹ، ایم. ایک ناول سی ٹرمینل لوکلائزیشن شکل کے ذریعے مائٹوکونڈریا کو ہیپاٹائٹس سی وائرس کور پروٹین کو نشانہ بنانا۔ جے ویرول۔ 2004، 78، 7958–7968۔ [کراس ریف] [پب میڈ]
25. کوریناگا، ایم۔ وانگ، ٹی. لی، وائی۔ شوالٹر، ایل اے؛ چان، ٹی. سن، جے؛ وین مین، SA ہیپاٹائٹس سی وائرس کور پروٹین مائٹوکونڈریل الیکٹران کی نقل و حمل کو روکتا ہے اور رد عمل آکسیجن پرجاتیوں (ROS) کی پیداوار کو بڑھاتا ہے۔ J. Biol کیم 2005، 280، 37481–37488۔ [کراس ریف] [پب میڈ]
26. ماچیدا، K.؛ چینگ، کے ٹی؛ لائ، سی کے؛ جینگ، کے ایس؛ گایا، VM؛ لائی، ایم ایم ہیپاٹائٹس سی وائرس ری ایکٹو آکسیجن پرجاتیوں کی پیداوار کے ساتھ مائٹوکونڈریل پارگمیٹی ٹرانزیشن کو متحرک کرتا ہے، جس سے ڈی این اے کو نقصان ہوتا ہے اور STAT3 ایکٹیویشن ہوتا ہے۔ جے ویرول۔ 2006، 80، 7199–7207۔ [کراس ریف] [پب میڈ]
27. وانگ، ٹی. کیمبل، آر وی؛ یی، ایم کے؛ لیموں، ایس ایم؛ وائن مین، SA وائرل سے متاثرہ مائٹوکونڈریل dysfunction میں ہیپاٹائٹس سی وائرس کور پروٹین کا کردار۔ جے وائرل۔ ہیپاٹ۔ 2010، 17، 784–793۔ [کراس ریف]
28. کم، ایس جے؛ سید، جی ایچ؛ خان، ایم؛ چیو، ڈبلیو ڈبلیو؛ سہیل، ایم اے؛ گش، آر جی؛ صدیقی، اے۔ ہیپاٹائٹس سی وائرس مائٹوکونڈریل فیشن کو متحرک کرتا ہے اور وائرل استقامت کو فروغ دینے کے لیے اپوپٹوس کو کم کرتا ہے۔ پروک ناٹل اکاد۔ سائنس USA 2014, 111, 6413–6418. [کراس ریف]
29. Siu, GK; چاؤ، ایف۔ یو، ایم کے؛ ژانگ، ایل. وانگ، ٹی. لیانگ، Y. چن، وائی؛ چان، ہائی کورٹ؛ Yu, S. ہیپاٹائٹس سی وائرس NS5A پروٹین phosphatidylinositol 4-kinase III کے ساتھ مائٹوکونڈریل فریگمنٹیشن کو آمادہ کرتا ہے۔ سائنس Rep. 2016, 6, 23464. [CrossRef]
30. حرا، وائی. یاناتوری، آئی۔ اکیڈا، ایم؛ Kiyokage, E.; نشینا، ایس. Tomiyama, Y.; Toida, K.; کیشی، ایف. کاٹو، این. امامورا، ایم. ET رحمہ اللہ تعالی. ہیپاٹائٹس سی وائرس کور پروٹین مائٹوکونڈریل ڈیپولرائزیشن کے تناظر میں پارکن کے ساتھ تعامل کرکے مائٹوفجی کو دباتا ہے۔ ایم۔ جے پاتھول۔ 2014، 184، 3026–3039۔ [کراس ریف]
31. گو، ایچ. زاؤ، ایم؛ سو، ایچ. یوآن، جے؛ وہ W.؛ Zhu, M.; ڈنگ، ایچ. یی، ایل۔ چن، جے سی ایس ایف وی نے اپوپٹوس کو روکنے کے لیے مائٹوکونڈریل فیشن اور مائٹوفگی کی حوصلہ افزائی کی۔ Oncotarget 2017, 8, 39382–39400۔ [کراس ریف]
32. فین، ایس. وو، کے؛ زاؤ، ایم؛ یوآن، جے؛ ما، ایس. Zhu, E.; چن، وائی؛ ڈنگ، ایچ. یی، ایل۔ چن، J. LDHB روکنا مائٹوفجی کو اکساتا ہے اور CSFV انفیکشن کے بڑھنے میں سہولت فراہم کرتا ہے۔ آٹوفیجی 2020، 16، 1-20۔ [کراس ریف] [پب میڈ]
33. غذائی، بی. زاؤ، ایم؛ گانا، ڈی. وو، کے؛ یی، ایل۔ لی، ڈبلیو. لی، ایکس۔ وانگ، کے؛ چن، J. آٹوفجی کی شمولیت اور CSFV کے ذریعے قسم I IFN سراو کو دبانا۔ آٹوفیجی 2020، 16، 1–23۔ [کراس ریف]
34. باربیئر، وی. لینگ، ڈی. Valois, S.; Rothman, AL; میڈین، CL ڈینگی وائرس Drp1-متحرک مائٹوکونڈریل فِشن کی خرابی کے ذریعے مائٹوکونڈریل لمبا ہونے کو اکساتا ہے۔ وائرولوجی 2017، 500، 149–160۔ [کراس ریف]
35. یو، سی وائی؛ لیانگ، جے جے؛ لی، جے کے؛ لی، وائی ایل؛ چانگ، بی ایل؛ Su, CI; ہوانگ، ڈبلیو جے؛ لائی، ایم ایم؛ لن، وائی ایل ڈینگی وائرس مائٹوفوسینز کو صاف کرکے مائٹوکونڈریل فیوژن کو متاثر کرتا ہے۔ پی ایل او ایس پیتھوگ۔ 2015، 11، e1005350۔ [کراس ریف]
36. یو، وائی ایس؛ پارک، وائی جے؛ لی، ایچ ایس؛ Oanh, NTK; Cho, MY; ہیو، جے؛ لی، ای ایس؛ چو، ایچ. پارک، YY؛ Cho, H. Mitochondria ubiquitin ligase, 5 مارچ کو جگر کے روگجنن میں ہیپاٹائٹس بی وائرس X پروٹین کے مجموعوں کو حل کرتا ہے۔ سیل ڈیتھ ڈس۔ 2019، 10، 938۔ [کراس ریف] [پب میڈ]
37. کم، ایس جے؛ خان، ایم؛ کوان، جے؛ تک، A.؛ سبرامانی، ایس. صدیقی، اے۔ ہیپاٹائٹس بی وائرس مائٹوکونڈریل ڈائنامکس میں خلل ڈالتا ہے: اپوپٹوسس کو کم کرنے کے لیے فیشن اور مائٹوفجی کو اکساتا ہے۔ پی ایل او ایس پیتھوگ۔ 2013، 9، e1003722۔ [کراس ریف] [پب میڈ]
38. چن، ڈبلیو. کالوو، PA؛ Malide, D.; گبز، جے؛ شوبرٹ، یو۔ Bacik، I.؛ بستا، ایس. O'Neill, R.; Schickli، J.؛ Palese, P.; ET رحمہ اللہ تعالی. ایک ناول انفلوئنزا اے وائرس مائٹوکونڈریل پروٹین جو سیل کی موت کو اکساتا ہے۔ نیٹ میڈ. 2001، 7، 1306–1312۔ [کراس ریف]
39. گبز، جے ایس؛ Malide, D.; ہورننگ، ایف۔ بیننک، جے آر؛ Yewdell, JW انفلوئنزا اے وائرس PB1-F2 پروٹین اندرونی مائٹوکونڈریل جھلی کو ایک پیش گوئی شدہ بنیادی ایمفیپیتھک ہیلکس کے ذریعے نشانہ بناتا ہے جو مائٹوکونڈریل فنکشن میں خلل ڈالتا ہے۔ جے ویرول۔ 2003، 77، 7214–7224۔ [کراس ریف]
40. یمادا، ایچ. Chounan, R.; Higashi, Y.; Kurihara، N.؛ Kido، H. مائٹوکونڈریل انفلوئنزا A وائرس PB1-F2 پروٹین اور مائٹوکونڈریا میں اس کا کام کا ہدف سازی کی ترتیب۔ FEBS Lett. 2004، 578، 331–336۔ [کراس ریف] [پب میڈ]
41. یوشیزومی، ٹی. Ichinohe, T.; ساساکی، او۔ اوٹیرا، ایچ. Kawabata, S.; میہارا، کے. کوشیبا، T. انفلوئنزا اے وائرس پروٹین PB1-F2 Tom40 چینلز کے ذریعے مائٹوکونڈریا میں منتقل ہوتا ہے اور پیدائشی قوت مدافعت کو کمزور کرتا ہے۔ نیٹ کمیون 2014، 5، 4713۔ [کراس ریف]
42. وانگ، آر. Zhu, Y.; رین، سی. یانگ، ایس. تیان، ایس. چن، ایچ. جن، ایم؛ Zhou, H. Inffluenza A وائرس پروٹین PB1-F2 مائٹوفجی کو آمادہ کرکے پیدائشی قوت مدافعت کو کمزور کرتا ہے۔ آٹوفیجی 2021، 17، 496–511۔ [کراس ریف]
43. Pila-Castellanos, I.; Molino, D.; میک کیلر، جے؛ لائنز، ایل. دا گراکا، جے؛ Tauziet، M.؛ چنٹیلوپ، ایل۔ Mikaelian, I.; Meyniel-Schicklin, L.; کوڈوگنو، پی۔ ET رحمہ اللہ تعالی. ایک نئی اینٹی وائرل حکمت عملی کے طور پر انفلوئنزا وائرس کے انفیکشن کی وجہ سے مائٹوکونڈریل مورفوڈینامکس تبدیلی۔ پی ایل او ایس پیتھوگ۔ 2021, 17, e1009340۔
44. Cornillez-Ty, CT; لیاو، ایل. یٹس، جے آر، تیسرا؛ کوہن، پی. Buchmeier، MJ شدید ایکیوٹ ریسپائریٹری سنڈروم کورونا وائرس نان اسٹرکچرل پروٹین 2 ایک میزبان پروٹین کمپلیکس کے ساتھ بات چیت کرتا ہے جو مائٹوکونڈریل بائیوجنسیس اور انٹرا سیلولر سگنلنگ میں شامل ہے۔ جے ویرول۔ 2009، 83، 10314–10318۔ [کراس ریف]
45. مرک ورتھ، سی۔ لینجر، ٹی مائٹوکونڈریا کے اندر پرہیبٹین کا فنکشن: سیل کے پھیلاؤ اور کرسٹی مورفوجینیسیس کے لیے ضروری کردار۔ بائیوکیم۔ بائیوفیس۔ ایکٹا 2009، 1793، 27–32۔ [کراس ریف]
46. ش، سی ایس؛ Qi, HY; بولران، سی.؛ ہوانگ، NN؛ ابو اصاب، ایم. Shelhamer, JH; Kehrl، JH SARS-کورونا وائرس اوپن ریڈنگ فریم-9b مائٹوکونڈریا اور MAVS/TRAF3/TRAF6 سگنلزوم کو نشانہ بنا کر پیدائشی قوت مدافعت کو دباتا ہے۔ J. Immunol. 2014، 193، 3080–3089۔ [کراس ریف] [پب میڈ]
47. سنگھ، ایم. بنسل، وی. Feschotte, C. انسانی کورونا وائرس کے داخلے کے عوامل کا ایک سنگل سیل RNA اظہار کا نقشہ۔ سیل کا نمائندہ 2020، 32، 108175۔ [CrossRef] [PubMed]
48. گورڈن، ڈی ای؛ جنگ، جی ایم؛ Bouhaddou, M.; سو، جے؛ Obernier, K.; سفید، کلومیٹر؛ O'Meara، MJ؛ Rezelj, VV; گو، جے زیڈ؛ سوانی، ڈی ایل؛ ET رحمہ اللہ تعالی. ایک SARS-CoV-2 پروٹین کے تعامل کا نقشہ منشیات کے دوبارہ استعمال کے اہداف کو ظاہر کرتا ہے۔ فطرت 2020، 583، 459–468۔ [کراس ریف] [پب میڈ]
49. آشیان، ڈی. جیانگ، ایکس؛ مورگن، ڈی جی؛ ہیوزر، جے ای؛ وانگ، ایکس؛ Akey، CW اپوپٹوسم کی تین جہتی ساخت: اسمبلی، پروکاسپیس-9 بائنڈنگ، اور ایکٹیویشن کے لیے مضمرات۔ مول سیل 2002، 9، 423–432۔ [کراس ریف]
50. نومورا تاکیگاوا، وائی۔ ناگانو-فوجی، ایم. ڈینگ، ایل. Kitazawa, S.; Ishido, S.; صدا، کے. ہوٹا، ایچ۔ ہیپاٹائٹس سی وائرس کا غیر ساختی پروٹین 4A مائٹوکونڈریا پر جمع ہوتا ہے اور خلیوں کو مائٹوکونڈریا کی ثالثی اپوپٹوس سے گزرنے کا خطرہ بناتا ہے۔ جے جنرل ویرول 2006، 87، 1935–1945۔ [کراس ریف] [پب میڈ]
51. Chiou, HL; Hsieh, YS; Hsieh, MR; چن، TY HCV E2 مائٹوکونڈریل سے متعلق کیسپیس پاتھ وے کے ذریعے Huh-7 خلیوں کے apoptosis کو آمادہ کر سکتا ہے۔ بائیو کیم۔ بائیوفیس۔ Res. کمیون 2006، 345، 453–458۔ [کراس ریف]
52. لی، ایس کے؛ پارک، SO؛ جو، CO؛ کم، وائی ایس ایچ سی وی کور پروٹین کا 14-3-3 ایپسیلون پروٹین کے ساتھ تعامل اپوپٹوس کو چالو کرنے کے لیے Bax کو جاری کرتا ہے۔ بائیو کیم۔ بائیوفیس۔ Res. کمیون 2007، 352، 756–762۔ [کراس ریف] [پب میڈ]
53. زاؤ، ص. ہان، ٹی. گو، جے جے؛ Zhu, SL; وانگ، جے؛ Ao, F.; جینگ، ایم زیڈ؛ وہ، YL؛ وو، زیڈ ایچ؛ ہاں، LB HCV NS4B مائٹوکونڈریل موت کے راستے کے ذریعے اپوپٹوس کو اکساتا ہے۔ وائرس ریس 2012، 169، 1–7۔ [کراس ریف] [پب میڈ]
54. جاوید، ایف. منظور، S. HCV غیر ساختی NS4A جینوٹائپ 3a پروٹین بیکس اور کیسپیس جھرن کو چالو کر کے مائٹوکونڈریا میں ثالثی موت کو آمادہ کرتا ہے۔ مائکروب پیتھوگ 2018، 124، 346–355۔ [کراس ریف] [پب میڈ]
55. تکاڈا، ایس. شیراکتا، وائی۔ کنینیوا، این۔ Koike، K. مائٹوکونڈریا کے ساتھ ہیپاٹائٹس بی وائرس ایکس پروٹین کی ایسوسی ایشن جوہری دائرہ میں مائٹوکونڈریل ایگریگیشن کا سبب بنتی ہے، جس سے خلیات کی موت ہوتی ہے۔ اونکوجین 1999، 18، 6965–6973۔ [کراس ریف] [پب میڈ]
56. ناصرالدین، AM؛ وانگ، ایل. لیو، ڈی ایکس انڈکشن آف p53-ڈیپینڈنٹ اور مائٹوکونڈریا میڈیٹیڈ سیل ڈیتھ پاتھ وے بذریعہ ڈینگی وائرس انسانوں اور حیوانی خلیوں کے انفیکشن۔ جرثومے متاثر کرتے ہیں۔ 2008، 10، 1124–1132۔ [کراس ریف]
57. گاو، ڈبلیو وائی؛ ڈھکن.؛ Cai, DE; ہوانگ، XY؛ Zheng, BY; ہوانگ، YH؛ چن، زیڈ ایکس؛ وانگ، XZ ہیپاٹائٹس بی وائرس X پروٹین HL-7702 خلیوں کو مائٹوکونڈریل پارگمیبلٹی ٹرانزیشن پور کی ماڈیولیشن کے ذریعے آکسیڈیٹیو تناؤ سے متاثرہ اپوپٹوسس کے لیے حساس بناتا ہے۔ اونکول۔ نمائندہ 2017، 37، 48–56۔ [کراس ریف] [پب میڈ]
58. کم، ایچ جے؛ کم، ایس وائی؛ کم، جے؛ لی، ایچ. چوئی، ایم؛ کم، جے کے؛ آہن، جے کے ہیپاٹائٹس بی وائرس ایکس پروٹین بیکس کو مائٹوکونڈریا میں ٹرانسلوکیشن بڑھا کر اپوپٹوس کو اکساتا ہے۔ IUBMB لائف 2008, 60, 473–480۔ [کراس ریف]
59. پادھن، K. میناکشی، آر. توحید، MAB؛ جمیل، S. شدید ایکیوٹ ریسپائریٹری سنڈروم کورونا وائرس 3a پروٹین p38 MAP کناز ایکٹیویشن کے ذریعے مائٹوکونڈریل موت کے راستے کو متحرک کرتا ہے۔ جے جنرل ویرول 2008، 89، 1960–1969۔ [کراس ریف] [پب میڈ]
60. ژانگ، ایل. وی، ایل. جیانگ، ڈی. وانگ، جے؛ کانگریس، ایکس۔ Fei, R. SARS-CoV نیوکلیو کیپسڈ پروٹین induced apoptosis of COS-1 ثالثی مائٹوکونڈریل پاتھ وے کے ذریعے۔ آرٹیف خلیات خون کے متبادل۔ متحرک بائیو ٹیکنالوجی 2007، 35، 237–253۔ [کراس ریف]
61. Chan, CM; ما، سی ڈبلیو؛ چان، ڈبلیو وائی؛ چان، ایچ وائی سارس-کورونا وائرس میمبرین پروٹین اکٹ کی بقا کے راستے کو ماڈیول کرنے کے ذریعے اپوپٹوس کو اکساتا ہے۔ آرک بائیو کیم۔ بائیوفیس۔ 2007، 459، 197–207۔
62. گوریرو، آر. گوریرو، سی.؛ Acosta, O. Rotavirus Isolate Wt1-5 کے ساتھ انفیکشن کے ذریعے انسانی ایکیوٹ لیمفوبلاسٹک لیوکیمیا سیل لائن ریہ میں سیل کی موت کی شمولیت۔ بائیو میڈیسنز 2020، 8، 242۔ [کراس ریف] [پب میڈ]
63. Martin-Latil, S.; Mousson, L.; Autret, A.; Colbère-Garapin, F.; Blondel, B. Bax مائٹوکونڈریل پاتھ وے کے ذریعے روٹا وائرس سے متاثرہ اپوپٹوسس کے دوران چالو ہوتا ہے۔ جے ویرول۔ 2007، 81، 4457–4464۔ [کراس ریف] [پب میڈ]
64. بھومک، آر. ہلدر، یوسی؛ چٹوپادھیائے، ایس. نائک، ایم کے؛ چاولہ سرکار، ایم. روٹا وائرس انکوڈڈ نان اسٹرکچرل پروٹین 1 ٹیومر دبانے والے پروٹین p53 کو نشانہ بنا کر سیلولر اپوپٹوٹک مشینری کو ماڈیول کرتا ہے۔ جے ویرول۔ 2013، 87، 6840–6850۔ [کراس ریف]
65. مکھرجی، اے. پاترا، یو۔ بھومک، آر. چاولہ سرکار، ایم روٹا ویرل غیر ساختی پروٹین 4 انفیکشن کے دوران ڈائنامین سے متعلق پروٹین 1- منحصر مائٹوکونڈریل فریگمنٹیشن کو متحرک کرتا ہے۔ سیل مائکروبیول۔ 2018، 20، e12831۔ [کراس ریف] [پب میڈ]
66۔ زمرین، ڈی۔ گارسیا-سسترے، اے۔ Xiao, X.; وانگ، آر. Palese, P. انفلوئنزا وائرس PB1-F2 پروٹین مائٹوکون ڈرائل ANT3 اور VDAC1 کے ذریعے سیل کی موت کو اکساتا ہے۔ پی ایل او ایس پیتھوگ۔ 2005، 1، ای4۔ [کراس ریف]
67. یانگ، ایس. Gorshkov, K.; لی، ای ایم؛ سو، ایم؛ چینگ، وائی ایس؛ سورج، این. سہیلیان، ایف۔ ڈی ویل، این. منگ، جی؛ گانا، ایچ. ET رحمہ اللہ تعالی. مائٹوکونڈریل فریگمنٹیشن میں اضافہ کے ذریعے زیکا وائرس سے متاثر نیورونل اپوپٹوس۔ سامنے والا۔ مائکروبیول 2020، 11، 598203۔ [کراس ریف]
68. نیومن، ایس. El Maadidi, S.; فلیٹی، ایل۔ ہاون، ایف. لبیب، ایس. Schejtman, A.; مورر، یو۔ بورنر، سی۔ وائرس مائٹوکونڈریا میڈیٹیڈ اپوپٹوسس کو کیسے کنٹرول کرتے ہیں؟ وائرس ریس 2015، 209، 45–55۔ [کراس ریف] [پب میڈ]
69. Maiuri, MC; Zalckvar, E.; کمچی، اے. کرومر، جی خود کھانا اور خود کو مارنا: آٹوفیجی اور اپوپٹوسس کے درمیان کراسسٹالک۔ نیٹ Rev. Mol. سیل بائیول۔ 2007، 8، 741–752۔ [کراس ریف]
70. لی، ایس. وانگ، جے؛ چاؤ، اے. خان، ایف اے؛ Hu, L.; ژانگ، ایس پورسائن ری پروڈکٹیو اینڈ ریسپائریٹری سنڈروم وائرس اپوپٹوس کو کم کرنے کے لیے مائٹوکونڈریل فیشن اور مائٹوفجی کو متحرک کرتا ہے۔ Oncotarget 2016, 7, 56002–56012۔
71. مینگ، جی؛ زیا، ایم؛ وانگ، ڈی. چن، اے. وانگ، وائی؛ وانگ، ایچ. یو، ڈی. Wei, J. Mitophagy پھیپھڑوں کے کینسر کے خلیوں میں اندرونی apoptosis کو روک کر آنکولیٹک نیو کیسل بیماری کے وائرس کی نقل کو فروغ دیتا ہے۔ Oncotarget 2014, 5, 6365–6374.
72. Freundt, EC; یو، ایل. پارک، ای. لینارڈو، ایم جے؛ Xu، XN مالیکیولر تعین کرنے والے شدید ایکیوٹ ریسپائریٹری سنڈروم کورونا وائرس اوپن ریڈنگ فریم 3b پروٹین کے سب سیلولر لوکلائزیشن کے لیے۔ جے ویرول۔ 2009، 83، 6631–6640۔ [کراس ریف]
73. بوجکووا، ڈی. Klann, K.; کوچ، بی. کراؤس، ڈی. Ciesek, S.; Cinatl, J.; Münch, C. SARS-CoV-2-متاثرہ میزبان خلیوں کا پروٹومکس تھراپی کے اہداف کو ظاہر کرتا ہے۔ فطرت 2020، 583، 469–472۔ [کراس ریف] [پب میڈ]
74. میلان، ای. Curran، J.؛ Hofmann, K.; مراد پور، ڈی۔ بائنڈر، ایم. Bartenschlager, R.; Tschopp, J. Cardif RIG-I اینٹی وائرل پاتھ وے میں ایک اڈاپٹر پروٹین ہے اور اسے ہیپاٹائٹس سی وائرس کا نشانہ بنایا جاتا ہے۔ فطرت 2005، 437، 1167–1172۔ [کراس ریف] [پب میڈ]
75. لی، ایکس ڈی؛ سورج، ایل. سیٹھ، آر بی؛ پینیڈا، جی؛ چن، زیڈ جے ہیپاٹائٹس سی وائرس پروٹیز NS3/4A پیدائشی قوت مدافعت سے بچنے کے لیے مائٹوکونڈریا سے مائٹوکونڈریل اینٹی وائرل سگنلنگ پروٹین کو توڑ دیتا ہے۔ پروک ناٹل اکاد۔ سائنس USA 2005, 102, 17717–17722۔ [کراس ریف] [پب میڈ]
76. فینگ، ایچ. سینڈر، AL؛ Moreira-Soto, A.; یمانے، ڈی۔ ڈریکسلر، جے ایف؛ لیمن، ایس ایم ہیپاٹو وائرس 3 اے بی سی پروٹیز اور مائٹوکونڈریل اینٹی وائرل سگنلنگ پروٹین (ایم اے وی ایس) کا ارتقاء۔ جے ہیپاٹول۔ 2019، 71، 25-34۔ [کراس ریف] [پب میڈ]
77. Qian, S.; فین، ڈبلیو. لیو، ٹی. وو، ایم؛ ژانگ، ایچ. Cui، X. Zhou, Y.; Hu, J.; وی، ایس؛ چن، ایچ. ET رحمہ اللہ تعالی. سینیکا ویلی وائرس کلیویج کے لیے اڈاپٹر پروٹین MAVS، TRIF، اور TANK کو ہدف بنا کر میزبان قسم I انٹرفیرون کی پیداوار کو دباتا ہے۔ جے ویرول۔ 2017، 91، ای00823-17۔ [کراس ریف] [پب میڈ]
78. وی، سی. نی، سی۔ گانا، ٹی. لیو، وائی؛ یانگ، ایکس؛ زینگ، زیڈ؛ جیا، وائی۔ یوآن، Y. گوان، K.؛ Xu, Y.; ET رحمہ اللہ تعالی. ہیپاٹائٹس بی وائرس ایکس پروٹین مائٹوکونڈریل اینٹی وائرل سگنلنگ پروٹین کو کم کرکے فطری قوت مدافعت میں خلل ڈالتا ہے۔ J. Immunol. 2010، 185، 1158–1168۔ [کراس ریف]
79. سورج، Y. زینگ، ایچ. یو، ایس. ڈنگ، وائی۔ وو، ڈبلیو؛ ماؤ، ایکس۔ لیاو، وائی؛ مینگ، سی. الرحمن، Z. ٹین، ایل. ET رحمہ اللہ تعالی. نیو کیسل ڈیزیز وائرس V پروٹین E3 Ubiquitin Ligase RNF5 کے ذریعے میزبان قسم I انٹرفیرون کی پیداوار کو روکنے کے لیے مائٹوکونڈریل اینٹی وائرل سگنلنگ پروٹین کو کم کرتا ہے۔ جے ویرول۔ 2019، 93، ای00322-19۔ [کراس ریف]
80. ڈنگ، ایس. Zhu, S.; رین، ایل. فینگ، این. گانا، Y. جی، ایکس۔ لی، بی؛ Flavell, RA; گرینبرگ، HB Rotavirus VP3 آنتوں کے اپکلا خلیوں میں قسم III انٹرفیرون اظہار کو روکنے کے لیے انحطاط کے لیے MAVS کو نشانہ بناتا ہے۔ Elife 2018, 7, e39494. [کراس ریف] [پب میڈ]
